
【题目】根据题目要求完成填空:
(1)下列物质中,电解质;非电解质A.氢氧化钠溶液 B.液氨 C.氯化钠晶体 D.二氧化碳 E.硫酸钡
(2)100mLFe2(SO4)3溶液中含有Fe3+11.2g,其中铁离子的物质的量n(Fe3+)= , 硫酸根离子的物质的量浓度c(SO ![]() )= , 取25mL溶液稀释到100mL,则稀释后溶液中Fe3+的物质的量浓度是c(Fe3+)= , 稀释后溶液中Fe2(SO4)3的质量m= .
)= , 取25mL溶液稀释到100mL,则稀释后溶液中Fe3+的物质的量浓度是c(Fe3+)= , 稀释后溶液中Fe2(SO4)3的质量m= .
【答案】
(1)CE;BD
(2)0.2mol;3mol/L;0.5mol/L;10g
【解析】解:(1)A.氢氧化钠溶液是混合物,既不是电解质也不是非电解质; B.液氨溶于水或熔融态时自身不能发生电离,是非电解质; C.氯化钠晶体溶于水后能够发生电离,溶液导电,是电解质; D.二氧化碳溶于水或熔融态时自身不能发生电离,是非电解质; E.硫酸钡熔融态时能够发生电离而导电,是电解质;因此属于电解质的是CE,属于非电解质的是BD,所以答案是:CE;BD;(2)100mLFe2(SO4)3溶液中含有Fe3+11.2g,其中铁离子的物质的量n(Fe3+)= ![]() =0.2mol,在不考虑水解情况下,c(SO42﹣)=
=0.2mol,在不考虑水解情况下,c(SO42﹣)= ![]() c(Fe3+)=
c(Fe3+)= ![]() =
= ![]()
![]()
![]() =3mol/L,取25mL溶液稀释到100mL,则稀释后溶液中Fe3+的物质的量浓度是c(Fe3+)=
=3mol/L,取25mL溶液稀释到100mL,则稀释后溶液中Fe3+的物质的量浓度是c(Fe3+)= ![]() =0.5mol/L,稀释后c(Fe2(SO4)3)=
=0.5mol/L,稀释后c(Fe2(SO4)3)= ![]() (Fe3+)=
(Fe3+)= ![]() ×0.5mol/L=0.25mol/L,稀释后溶液中Fe2(SO4)3的质量m=0.25mol/L×0.1L×400g/mol=10g,所以答案是:0.2mol;3mol/L;0.5mol/L;10g.
×0.5mol/L=0.25mol/L,稀释后溶液中Fe2(SO4)3的质量m=0.25mol/L×0.1L×400g/mol=10g,所以答案是:0.2mol;3mol/L;0.5mol/L;10g.


科目:高中化学 来源: 题型:
【题目】将一定量的SO2(g)和O2(g)分别通入到体积为2L的恒容密闭容器中,在不同温度下进行反应:2SO2(g)+O2(g)2SO3(g)△H<0.得到如表中的两组数据:

下列说法不正确的是( )
A. x=1.6,y=0.2,t<6 B. T1、T2的关系:T1>T2
C. K1、K2的关系:K2>K1 D. 实验1在前6 min的反应速率v (SO2)=0.2 molL﹣1min﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的分类或性质与应用均正确的是( )
A. Al2O3的熔点很高,可用于制作耐高温材料
B. Na2O2是碱性氧化物,具有强氧化性可用于杀菌消毒
C. 硅晶体是良好的半导体,可用于制造光导纤维
D. Al(OH)3是一种强碱,可以与酸反应,可用作医用的胃酸中和剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下发生反应:2X(g)![]() Y(g)+3Z(g) △H=akJ·mol-1(a>0)下列说法正确的是
Y(g)+3Z(g) △H=akJ·mol-1(a>0)下列说法正确的是
A. 增大X的浓度,正反应速率增大,逆反应速率减小
B. 将0.2molX充入反应器中,充分反应后,生成的Z的物质的量可能为0.09mol
C. 达到化学平衡状态时,正、逆反应的速率都为0
D. 达到化学平衡状态时,共吸收a kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题: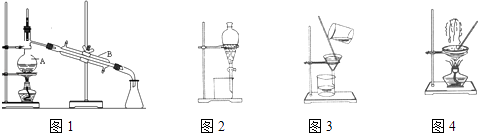
(1)装置图1中A的名称是 . A 中加入碎瓷片的作用是 .
(2)为了从海带中提取碘,某研究性学习小组设计并进行了以下实验: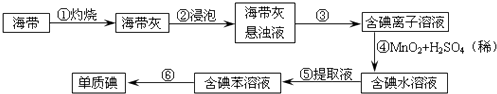
①灼烧海带时,除需要酒精灯与三脚架外,还需要用到的实验仪器是(从下列仪器中选出所需仪器,用标号字母填写在空白处);
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.铁架台 F.干燥器
②步骤③的实验选择上述装置图(填图的序号).步骤⑤的实验操作名称是 . 步骤⑥的目的是从含碘苯溶液中分离出单质碘,同时回收苯,该步骤的实验操作名称是 , 选择上述装置图(填图的序号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活处处有化学。下列说法正确的是( )
A. 制饭勺、饭盒、高压锅等的不锈钢是合金
B. 做衣服的棉和麻均与淀粉互为同分异构体
C. 煎炸食物的花生油和牛油都是高分子化合物
D. 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源问题日益成为制约国际社会经济发展的瓶颈。甲醇是一种可再生能源,具有广泛的开发和应用前景,因此甲醇被称为2l世纪的新型燃料。工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)![]() CH3OH(g)。图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图。
CH3OH(g)。图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图。
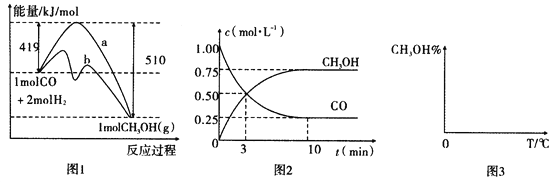
请回答下列问题:
(1)在“图1”中,曲线_____(填“a”或“b”)表示使用了催化剂;该反应属于______(填“吸热”或“放热”)反应。
(2)根据“图2”判断,下列说法不正确的是______________。
A.起始充入的CO为1mol
B.增加CO浓度,CO的转化率增大
C.容器中压强恒定时,反应已达平衡状态
D.保持温度和密闭容器容积不变,再充入1molCO和2molH2,再次达到平衡时n(CH3OH)/n(CO)会增大
(3)从反应开始到建立平衡,v(H2)=__________;该温度下CO(g)+2H2(g)![]() CH3OH(g)的化学平衡常数为___________。若保持其他条件不变,向平衡体系中再充入0.5mol CO、lmolH2、1.5 molCH3OH,此反应进行的方向为____________(填“正反应方向”或“逆反应方向)”。
CH3OH(g)的化学平衡常数为___________。若保持其他条件不变,向平衡体系中再充入0.5mol CO、lmolH2、1.5 molCH3OH,此反应进行的方向为____________(填“正反应方向”或“逆反应方向)”。
(4)请在“图3”中画出平衡时甲醇蒸气百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线__________(在曲线上标出p1、p2,且p1>p2)。
(5)科学家常用量热剂来直接测定某一反应的反应热,现测得:CH3OH(g)+3/2O2
(g)=CO2(g)+2H2O(g) △H=-192.9kJ/mol,又知H2O(l)=H2O(g)△H=+44 kJ/mol,请写出32g的CH3OH(g)完全燃烧生成液态水的热化学方程式_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com