
已知: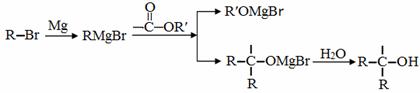
A是一种重要的化工原料,能使溴水反应褪色,且分子内所有的原子都在一条直线上,在不同的条件下,A可以转化为烃B和烃C,B和C的核磁共振氢谱中都只有一个吸收峰,B能使溴水反应褪色而C不能使溴水反应褪色。A~J分别代表一种有机物,并有如下的转化关系:
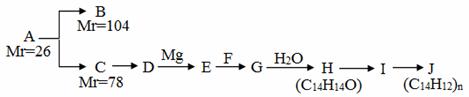
回答下列问题:
(1)A的结构简式为________________;
(2)B的结构简式为_________________;
(3)反应C→D所需要的试剂是_________________________;
(4)H不能发生催化氧化,H的结构简式是____________________________________;
(5) I中的官能团名称是___________________;
(6) I中可能含有的杂质是_____________________(写结构简式);
(7)写出I→J的反应方程式________________________________________________;
(8)H有多种同分异构体,符合下列条件的同分异构体有________种。
①能与FeCl3溶液显紫色;②有二联苯结构;③二联苯上有两个侧链。
其中核磁共振氢谱中吸收峰最少的结构简式是____________________________。
科目:高中化学 来源: 题型:
在某温度下,将2molA和3molB充入一密闭容器中,发生反应:aA(g)+B(g) 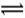 C(g)+D(g),5min后达到平衡,各物质的平衡浓度有如下关系:c
C(g)+D(g),5min后达到平衡,各物质的平衡浓度有如下关系:c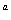 (A)×c(B)=c(C) ×c(D)。若在此温度下,将容器的体积扩大为原来的10倍,B的转化率不变,则此时A的转化率( )
(A)×c(B)=c(C) ×c(D)。若在此温度下,将容器的体积扩大为原来的10倍,B的转化率不变,则此时A的转化率( )
A.60% B.40% C.20% D.10%
查看答案和解析>>
科目:高中化学 来源: 题型:
化学反应N2+3H2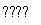 2NH3的能量变化如图所示,该反应的热化学方程式是 )。
2NH3的能量变化如图所示,该反应的热化学方程式是 )。
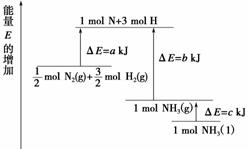
A.N2g)+3H2g)2NH3l) ΔH=2a-b-c)kJ·mol-1
B.N2g)+3H2g)2NH3g) ΔH=2b-a)kJ·mol-1
C.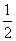 N2g)+
N2g)+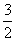 H2g)NH3l) ΔH=b+c-a)kJ·mol-1
H2g)NH3l) ΔH=b+c-a)kJ·mol-1
D.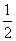 N2g)+
N2g)+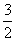 H2g)NH3g) ΔH=a+b)kJ·mol-1
H2g)NH3g) ΔH=a+b)kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是
A.铅蓄电池的缺点是比能量低、笨重,废弃电池污染环境
B.做衣服的棉和麻均与淀粉互为同分异构体
C.大量燃烧化石燃料是造成雾霾天气的一种重要因素
D.煎炸食物的花生油和牛油都是可皂化的酯类
查看答案和解析>>
科目:高中化学 来源: 题型:
S2Cl2是一种重要的化工产品。常温时是一种有毒并有恶臭的金黄色液体,熔点-76℃,沸点138℃,易与水反应,进一步氯化可得SCl2,SCl2是樱桃红色液体,易挥发,熔点-122℃,沸点59℃。SCl2 与S2Cl2相似,有毒并有恶臭,但更不稳定。S2Cl2可用下列装置制备。
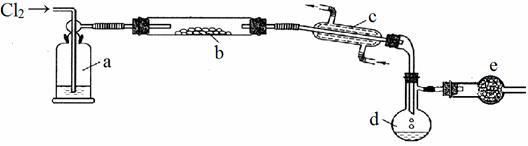
回答下列问题:
(1)写出S2Cl2的电子式_____________________;
(2)写出指定仪器的名称c___________________,d_________________________;
(3)a瓶盛放的试剂是_______________________ ;
(4)b中的反应开始前,需排除装置中的空气,应采取的方法是:_______________________;
(5)装置e中盛放的试剂是_____________其作用是①______________________________ ②___________________________________;
(6)得到纯净的S2Cl2,需要进行的操作是__________;
(7)若将S2Cl2放入水中同时产生沉淀和气体写出反应的方程式
___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示, 为直流电源,
为直流电源, 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽。接通电路(未闭合K)后发现
为电镀槽。接通电路(未闭合K)后发现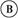 上的c点显红色。为实现铁片上镀铜,接通K后,使c、d两点短路。下列叙述不正确的是( )
上的c点显红色。为实现铁片上镀铜,接通K后,使c、d两点短路。下列叙述不正确的是( )
A.b为直流电源的负极
B.f极为阴极,发生还原反应
C.e极材料为铁片,f极材料的铜片
D.可选用CuSO4溶液或CuCl2溶液作电镀液
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是某兴趣小组在实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。
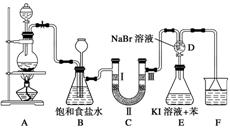
(1)实验室制备氯气的化学方程式为_____________________________________________,
该反应的氧化剂是____________。
(2)装置B中饱和食盐水的作用是______________________________________________;
同时装置B亦是安全瓶,监测实验进行时装置C是否发生堵塞,请写出发生堵塞时装置B中的现象:________________________________________________________________。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此装置C中Ⅰ、Ⅱ、Ⅲ处依次放入________(填“a”、“b”、“c”或“d”)。
| a | b | c | d | |
| Ⅰ | 干燥的有 色布条 | 干燥的有 色布条 | 湿润的有 色布条 | 湿润的有 色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有 色布条 | 湿润的有 色布条 | 干燥的有 色布条 | 干燥的有 色布条 |
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性强弱。
向装置D中缓缓通入少量氯气时,可以看到________,说明氯的非金属性大于溴。打开活塞,将装置D中的少量溶液加入装置E中,振荡。观察到E中溶液分为两层,上层(苯层)为紫红色,说明溴的非金属性______碘。
(5)下列装置中可以代替装置F的是________。
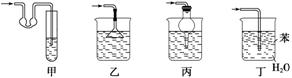
查看答案和解析>>
科目:高中化学 来源: 题型:
下列具有特殊性能的材料中,由主族元素和副族元素形成的化合物是( )。
A.吸氢材料镧镍合金 B.半导体材料砷化镓
C.高温结构陶瓷材料氮化硅 D.透明陶瓷材料硒化锌
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨的温度和压强通常控制在约500℃以及20 MPa~50 MPa的范围,当进入合成塔的N2和H2的体积比为1∶3时,经科学实验测定,在相应条件下N2和H2反应所得氨的平衡浓度(体积分数)如下表所示:

而实际上从合成塔出来的混合气体中含有氨约为15%。
请回答下列问题:
(1)298 K下合成氨时,每生成1 mol 氨气,同时放出46.2 kJ的热量,则该反应的热化学方程式为_________________________________________________。
氨气,同时放出46.2 kJ的热量,则该反应的热化学方程式为_________________________________________________。
在该温度下,取1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在的条件下进行反应,测得反应放出的热量总小于92.4 kJ,其原因是______________。
(2)实际上从合成塔出来的混合气体中氨的体积分数小于理论值的根本原因是_______________。
A.表中所测数据有明显误差
B.生产条件控制不当
C.氨的分解速率大于预测值
D.合成塔中的反应未达到平衡状态
(3)若工业生产中N2和H2按投料比1∶2.8的比例进入合成塔,那么转化率较大的应该是_________,采用此投料比的原因是______________,
若从合成塔出来的混合气体中氨的体积分数仍为15%,则N2和H2的转化率之比是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com