
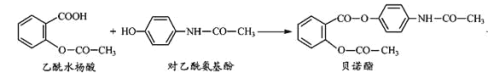
【题目】药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得。下列叙述正确的是( )
 +H2O
+H2O
A.贝诺酯分子中有三种含氧官能团
B.贝诺酯与足量 NaOH 溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠
C.乙酰水杨酸和对乙酰氨基酚均能与 NaHCO3溶液反应
D.可用 FeCl3 溶液区别乙酰水杨酸和对乙酰氨基酚
科目:高中化学 来源: 题型:
【题目】汽车尾气中含有CO、NO、NO2、碳氢化合物等多种污染物。回答下列问题:
(1)汽车燃料中不含氮元素,尾气中所含NO产生的原因是_________________________(用化学方程式表示)。
(2)已知:2C4H10(g)+13O2(g)=8CO2(g)+10H2O(g) △H1=-5316 kJ·mol-1
N2(g)+O2(g)=2NO(g) △H2
2NO(g)+2CO(g)=N2(g)+2CO2(g) △H3=-746 kJ·mol-1
①若H2O(l)=H2O(g) △H=+44 kJ·mol-1,则表示正丁烷燃烧热的热化学方程式为__________________。
②部分化学键键能数据为:氧分子中氧氧键的键能为494 kJ·mol-1;C=O的键能为799 kJ·mol-1;CO分子中碳氧键的键能为1076 kJ·mol-1;请计算出反应2CO(g)+O2(g)=2CO2(g)的△H=______________kJ·mol-1,由此可以计算△H2=__________kJ·mol-1
(3)1573K时,N2+O2![]() 2NO平衡常数为2.0×10-6,若测得内燃机内平衡混合气中氮气、氧气的物质的量分别为0.2mol、0.001mol,则生成NO的物质的量为_____________mol,N2的转化率为____________。
2NO平衡常数为2.0×10-6,若测得内燃机内平衡混合气中氮气、氧气的物质的量分别为0.2mol、0.001mol,则生成NO的物质的量为_____________mol,N2的转化率为____________。
(4)T<500K时,反应NO2(g)+CO(g)=NO(g)+CO2(g)分两步进行:
第一步:NO2(g)+NO2(g)=NO3(g)+NO(g) (慢反应)
第二步:NO3(g)+CO(g)=NO(g)+CO2(g) (快反应)
下列表述正确的是__________(填标号)
A.反应速率与NO2浓度有关 B.反应速率与NO浓度有关
C.反应的中间产物只有NO3 D.第一步反应活化能较低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图如图,其中电解池中隔膜仅阻止气体通过,阴、阳极均为石墨电极。下列相关叙述正确的是
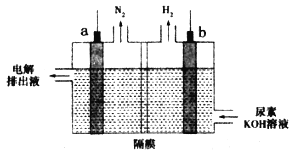
A.b电极为阳极
B.电子由b电极经过溶液流入a电极形成回路
C.b电极上发生失去电子的反应
D.尿素在a电极发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是
A. HCl和NaOH反应的中和热△H=-57.3 kJ·mol1,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ·mol1
B. 甲烷的标准燃烧热ΔH=-890.3 kJ·mol1,则CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH<-890.3 kJ·mol1
C. 已知:500℃、30MPa下,N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4kJ·mol-1;将1.5 mol H2和过量的N2在此条件下充分反应,放出热量46.2 kJ
2NH3(g) ΔH=-92.4kJ·mol-1;将1.5 mol H2和过量的N2在此条件下充分反应,放出热量46.2 kJ
D. CO(g)的燃烧热是283.0kJ·mol1,则2CO2(g) ===2CO(g)+O2(g)反应的△H=+566.0 kJ·mol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)25℃时,浓度均为 0.10molL﹣1 的氨水和 NH4 Cl 溶液
①NH4 Cl 溶液显________性,原因是(用离子方程式表示)________,若加入少量的氨水,使溶液中 c(NH4+)=c(Cl-),则溶液的 pH________7 (填“>”、“<”或“=”).
②氨水显碱性的原因(用离子方程式表示)________,向氨水中加入 NH4Cl 固体,氨水的电离程度________(填“增大”、“减小”或“不变”),溶液的 pH 将________(填“增大”、“减小”或“不变”)。
(2)下列事实中,能说明 NH3·H2O弱碱的有________
①0.1 mol·L-1 NH3·H2O 溶液可以使酚酞试液变红
②0.1 mol·L-1 NH4Cl 溶液呈酸性
③0.1 mol·L-1NH3·H2O 溶液的导电能力比 0.1 mol·L-1NaOH 溶液弱
④等体积的 0.1 mol·L-1NH3·H O 溶液与 0.1 mol·L-1 HCl 溶液恰好完全反应
A.①②③ B.②③ C.②④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学工作者研发了一种 SUNCAT的系统,借助锂循环可持续,合成其原理如图所示。下列说法不正确的是
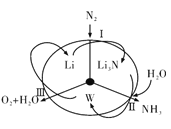
A. 过程I得到的Li3N的电子式为![]()
B. 过程Ⅱ生成W的反应为Li3N+3H2O=3LiOH+NH3↑
C. 过程Ⅲ涉及的阳极反应为4OH--4e-=O2↑+2H2O
D. 过程I、Ⅱ、Ⅲ均为氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧。活化过程的能量变化模拟计算结果如图所示。活化氧可以快速氧化SO2。下列说法正确的是( )
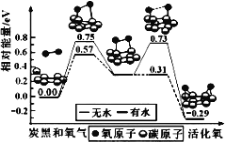
A.氧分子的活化是 O-O 的断裂与 C-O 键的生成过程
B.炭黑颗粒是大气中 SO2 转化为 SO3 的催化剂
C.每活化一个氧分子吸收 0.29eV 能量
D.水可使氧分子活化反应的活化能降低 0.42eV
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.c(H+)=![]() 的溶液一定呈中性
的溶液一定呈中性
B.将水加热,KW增大,pH不变,仍呈中性
C.向水中加入少量碳酸氢钠固体,溶液的c(H+) 增大,KW不变
D.向0.1mol·L-1醋酸溶液中加水,溶液中水电离产生的c(H+)将减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 、
、![]() 、
、![]() 、
、![]() 为原子序数依次增大的短周期元素,
为原子序数依次增大的短周期元素,![]() 为地壳中含量最高的过渡金属元素,
为地壳中含量最高的过渡金属元素,![]() 与
与![]() 同主族,
同主族,![]() 与
与![]() 同周期,且
同周期,且![]() 与
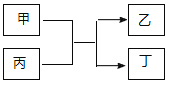
与![]() 的原子序数之和为20。甲、乙分别为元素E、A的单质, 丙、丁为A、E分别与B形成的二元化合物,它们转化关系如图所示。下列说法不正确的是( )
的原子序数之和为20。甲、乙分别为元素E、A的单质, 丙、丁为A、E分别与B形成的二元化合物,它们转化关系如图所示。下列说法不正确的是( )
A.![]() 、
、![]() 形成的一种化合物具有漂白性
形成的一种化合物具有漂白性
B.![]() 、
、![]() 形成的离子化合物可能含有非极性键
形成的离子化合物可能含有非极性键
C.![]() 的单质能与丙反应置换出
的单质能与丙反应置换出![]() 的单质
的单质
D.丁为黑色固体,且1mol甲与足量丙反应转移电子3 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com