
 如图示的原电池中,
如图示的原电池中,| 6.4g |
| 64g/mol |
| 0.2mol |
| 1L |


科目:高中化学 来源: 题型:
| A、2-丁炔 | B、丙炔 |
| C、1,3-戊二烯 | D、2-甲基丙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、二氧化硫可广泛用于食品的漂白 |
| B、碘是人体必需的微量元素,所以要多吃富含高碘酸的食物 |
| C、二氧化硅不与强酸反应,所以可用石英器皿盛放氢氟酸 |
| D、次氯酸钠溶液可用于环境的消毒杀菌 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、自然界中存在卤素单质 |
| B、随核电荷数增加,单质熔沸点升高 |
| C、随核电荷数增加,单质氧化性增强 |
| D、随核电荷数增加,氢化物稳定性增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
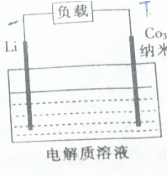 美国麻省理工学院科研人员通过改造M13病毒的基因,使病毒与金属结合后形成Co3O4纳米导线,然后用作电池的电极,从而大大提高了生产效率和电池的性能.这种富含Co3O4锂离子电池的反应原理为Co3O4+2Li
美国麻省理工学院科研人员通过改造M13病毒的基因,使病毒与金属结合后形成Co3O4纳米导线,然后用作电池的电极,从而大大提高了生产效率和电池的性能.这种富含Co3O4锂离子电池的反应原理为Co3O4+2Li| 放 |
| 充 |
| A、放电时,Li+向负极移动 |
| B、放电时,正极的电极反应式为Co3O4+2Li++2e-═2LiCoO2+Co, |
| C、充电时,Co3O4纳米线与外接电源负极相连 |
| D、充电时,阴极的电极反应式为Li-e-=Li+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 L 1 mol?L-1的NaClO 溶液中含有ClO-的数目为NA | ||
| B、钢铁的析氢腐蚀的负极反应:Fe-3e-=Fe3+ | ||
| C、判断一种电池的优劣标准是:电池的成本 | ||
D、向AlCl3溶液中滴加NaHCO3溶液,其离子反应方程式为:Al3++3HCO
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com