
下列离子方程式不能解释对应实验事实的是
A.向小苏打溶液滴加少量盐酸:HC03- +H+= H2O+CO2↑
B.用漂白液吸收过量SO2: SO2+H2O+ClO-=2H+ +SO42- +Cl-
C.将少量乙烯气体通入酸性KMnO4溶液:CH2 =CH2 +4H++MnO4—= C2O42-+Mn2++ 4H2O
D.将铜丝插入稀硝酸中:3Cu+8H++2N03一 =3Cu2++ 2NO↑ + 4H2O
科目:高中化学 来源:2014-2015学年湖南省怀化市高三学业水平模拟考试化学试卷(解析版) 题型:选择题
通常状况下下列气体遇到空气会发生颜色变化的是
A.N2 B.NH3 C.CO2 D.NO
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东高考佛山市高三二模理综化学试卷(解析版) 题型:选择题
下列实验操作、现象和结论均正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 向无色溶液中滴加氯水和CCl4,振荡静置 | 下层溶液显紫色 | 原溶液中含有I- |
B | 过量铁粉加入稀硝酸中充分反应,再加入KSCN溶液 | 溶液呈红色 | 稀硝酸将铁氧化为Fe2+ |
C | 向淀粉溶液中滴加稀硫酸,加热,取水解液少许,滴加银氨溶液,并水浴加热 | 没有银镜出现 | 淀粉没有发生水解 |
D | 用玻璃棒蘸取浓硫酸滴到蓝色石蕊试纸上 | 试纸变黑 | 浓硫酸具有脱水性 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省成都市高三4月模拟考理综化学试卷(解析版) 题型:选择题
下列图示与对应的叙述相符的是
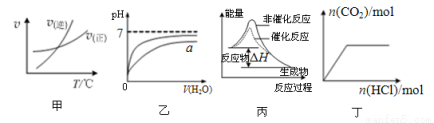
A.由图甲表示的反应速率随温度变化的关系可知该反应的ΔH>0
B.图乙表示pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应的是醋酸
C.图丙表示该反应为放热反应,且催化剂能改变反应的焓变
D.图丁表示向Na2CO3溶液中逐滴滴加稀盐酸,生成CO2与所加盐酸物质的量的关系
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省成都市第三次诊断化学试卷(解析版) 题型:填空题
(12分)某叶绿素的化学式为C55 H72N4O6Mg,其在人体代谢的中间产物为CO( NH:2)20。
(1)该叶绿素所含元素中,基态原子第一电离能最大的是 (填元素符号,下同);处于s区的元素有 。
(2)已知CO( NH2)2分子中C、N、O原子均达8电子稳定结构,其中N的杂化轨道类型为 ;在CO(NH2)2晶体中存在____ (填序号)o
A.非极性键 B.极性键 C.氢键 D.范德华力
(3)CO(NH2)2的熔点远远低于NaCl.其原因是 。
(4)工业上,用惰性电极电解法除去碱性溶液中的CO( NH2)2,产物均为无毒无害常见物质。则阳极除去CO(NH2)2的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆市高三下学期第一次月考理综化学试卷(解析版) 题型:实验题
(14分)化合物KxFe(C2O4)y·3H2O(Fe为+3价)是一种军用光敏材料,实验室可以用如下的方法来制备这种材料并测定这种材料的组成。
I.制备
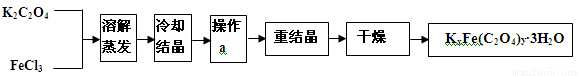
(1)结晶时应将饱和溶液用冰水冷却,同时放在黑暗处等待晶体的析出,这样操作的原因是____
(2)操作 a 名称是____
(3)称取一定质量的晶体置于锥形瓶中,加入足量蒸馏水和稀 H2SO4 ,将C2O42-转化为H2C2O4后用0.1100 mol/L KMnO4溶液滴定,当消耗 KMnO4溶液 24.00 mL 时恰好完全反应;再向溶液中加入适量的还原剂,恰好将 Fe3+完全转化为 Fe2+,用相同浓度的 KMnO4溶液继续滴定,当Fe2+完全氧化时,用去KMnO4溶液4.00 mL 。第二次滴定的离子方程式为 ,第二次滴定终点的现象为 。
(4)配制100 mL 0.1100 mol/L KMnO4溶液及滴定实验中所需的玻璃仪器除烧杯,玻璃棒、胶头滴管、量筒、锥形瓶外还有 (填仪器名称)。
(5)通过计算确定该材料的组成为: (填写化学式)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆市高三下学期第一次月考理综化学试卷(解析版) 题型:选择题
用下列装置进行相应实验,能达到实验目的的是
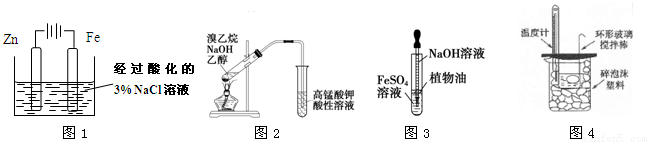
A.图1为牺牲阳极的阴极保护法,可以防止铁棒被腐蚀
B.图2所示装置可以检验溴乙烷与NaOH醇溶液共热产生的乙烯
C.图3所示装置可以用来制备氢氧化亚铁
D.图4所示装置可以用来测定中和热
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市高三四月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.将少量的溴水滴入FeCl2、NaI的混合溶液中,再滴加CCl4,振荡、静置,下层溶液呈紫红色,说明氧化性:Br2>Fe3+>I2
B.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=-57.3 kJ·mol-1,则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出57.3 kJ的热量
C.常温下,0.1 mol·L-1某一元酸HA溶液中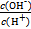 =1×10-12,溶液中加入一定量NaA晶体或加水稀释,溶液中c(OH-)均增大
=1×10-12,溶液中加入一定量NaA晶体或加水稀释,溶液中c(OH-)均增大
D.取久置的Na2O2粉末,向其中滴加过量的盐酸,产生无色气体,不能说明Na2O2是否变质
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三4月过程性检测理综化学试卷(解析版) 题型:填空题
选做(12分)【化学—物质结构与性质】N和B元素在化学中占有很重要的地位。
(1)写出N元素基态原子的价电子排布式_______。B、N和O元素的电负性由大到小的顺序为_______.
(2)N和B两元素氟化物的化学式相似,均为AB3型,但分子的空间结构有很大不同,其原因是___________,其中BF3的分子构型为_______________。
(3)BN的晶体结构与金刚石相似其中B原子的杂化方式为_______,微粒间存在的作用力是_________。
(4)根据电子云的重叠方式判断,N2分子中存在的σ键和π键数目之比为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com