
【题目】用VSEPR模型预测下列分子或离子的立体结构,其中不正确的是 ( )
A. BF4-为正四面体形
B. CO2为直线形
C. HCN为折线形(V形)
D. SO32-为三角锥形
 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源: 题型:
【题目】在2A+B3C+4D中,表示该反应速率最快的是( )
A.υ(A)=0.5molL﹣1S﹣1
B.υ(B)=0.3 molL﹣1S﹣1
C.υ(C)=0.8molL﹣1S﹣1
D.υ(D)=1 molL﹣1S﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如图所示.下列叙述中不正确的是( )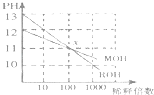
A.ROH是一种强碱
B.在x点,MOH并没有完全电离
C.在x点,c(M+)=c(R+)
D.稀释前,c(ROH)=10c(MOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验中不能直接测出石墨和氢气生成甲烷反应的反应热,但可测出甲烷,石墨,氢气燃烧的反应热:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1=﹣890.3kJ/mol
C(石墨)+O2(g)═CO2(g)△H2=﹣393.5kJ/mol
H2(g)+ ![]() O2(g)═H2O(l)△H3=﹣285.8kJ/mol,则由石墨生成甲烷的反应热:
O2(g)═H2O(l)△H3=﹣285.8kJ/mol,则由石墨生成甲烷的反应热:
C(石墨)+2H2(g)═CH4(g)△H4= .
查看答案和解析>>
科目:高中化学 来源: 题型:
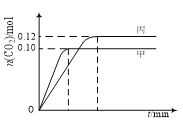
【题目】一定温度下,在三个容积均为2.0 L的恒容密闭容器中发生反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g)。各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如下图所示。下列说法正确的是
N2(g)+2CO2(g)。各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如下图所示。下列说法正确的是
容器 | 温度/℃ | 起始物质的量/mol | |
NO (g) | CO (g) | ||
甲 | T1 | 0.20 | 0.20 |
乙 | T1 | 0.30 | 0.30 |
丙 | T2 | 0.20 | 0.20 |
A. 该反应的正反应为吸热反应
B. 达到平衡时,乙中CO2的体积分数比甲中的大
C. T1℃时,若起始时向甲中充入0.40 mol NO、0.40mol CO、0.40mol N2和0.40mol CO2,则反应达到新平衡前v(正)<v(逆)
D. T2℃时,若起始时向丙中充入0.06mol N2和0.12 mol CO2,则达平衡时N2的转化率大于40%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了实现“将全球温度上升控制在2℃以内”,科学家正在研究温室气体CH4和CO2的转化和利用。
(1)下列说法正确的是__________(填序号)。
A. CH4与CO2分子均为含有极性共价键的非极性分子 B. 第一电离能:O>N>C
C. 沸点高低:CH4>SnH4>GeH4>SiH4 D. CH![]() 离子的空间构型为平面正三角形
离子的空间构型为平面正三角形
(2)CH4和CO2在Ni催化作用下反应可获得化工原料CO和H2。
①Ni基态原子核外电子排布式为__________。
②与CO互为等电子体的阴离子的电子式为__________,Ni能与CO形成正四面体形的配合物Ni(CO)4,1 mol Ni(CO)4中含有σ键的数目为__________。
(3)CH4和CO2在含有钛氧化物的某种催化剂作用下,可直接转化为CH3COOH。
①CH3COOH中C原子轨道杂化类型为__________;
②钛氧化物晶胞结构如图所示,写出其化学式:__________。
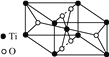
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池总反应的离子方程式为:2Fe3++Fe=3Fe2+ , 不能实现该反应的原电池是( )
A.正极为Fe,负极为Zn,电解质Fe2(SO4)3溶液
B.正极为Cu,负极为Fe,电解质FeCl3溶液
C.正极为Cu,负极为Fe,电解质Fe(NO3)3溶液
D.正极为Ag,负极为Fe,电解质Fe2(SO4)3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水开发利用的部分过程如图所示。下列说法错误的是

A. 向苦卤中通入Cl2是为了提取溴
B. 粗盐可采用除杂和重结晶等过程提纯
C. 工业生产中常选用NaOH作为沉淀剂
D. 富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com