
 、O
、O 、Ca
、Ca .
.分析 I.微粒间以分子间作用力结合形成的晶体为分子晶体,大多数共价化合物和非金属单质为分子晶体;微粒间以共价键结合形成空间网状结构的晶体为原子晶体,硅、二氧化硅、碳化硅、金刚石等属于原子晶体;阴阳离子之间通过离子键形成的晶体为离子晶体,活泼金属和活泼非金属形成的化合物一般为离子晶体,铵盐也属于离子晶体.
II.(4)根据原子结构示意图的书写方法来解答;
(5)根据具有双幻数的原子特别稳定;
(6)根据元素在周期表中的位置进行推断:原子序数为2、10、18、36、54、86、118,分别对应元素为第一、二、三、四、五、六、七周期的0族元素,114号可看成在118号元素的位置(第七周期的0族)再往前数四个位置来确定位置;根据具有双幻数的原子特别稳定.
解答 解:I.①MgCl2 ④NaCl ⑦Na2CO3⑨NaOH 这四种物质是由阴阳离子构成的,属离子晶体;
②干冰 ③冰 ⑤白磷(P4) 这三种物质是由分子构成的,属分子晶体,
⑥SiO2⑧金刚石 这两种物质是由原子构成的,属原子晶体;
故答案为:①④⑦⑨;②③⑤;⑥⑧;
II.(4)质子数为2、8、20的元素原子结构示意图分别为:He 、O
、O 、Ca
、Ca ,
,
故答案为:He 、O
、O 、Ca
、Ca ;
;
(5)168O的质子数为8,中子数为8,具有双幻数的原子尤为稳定,所以氧的同位素中原子核最稳定的是168O,故答案为:168O;
(6)原子序数为2、10、18、36、54、86、118,分别对应元素为第一、二、三、四、五、六、七周期的0族元素,114号可看成在118号元素的位置(第七周期的0族)再往前数四个位置,即为114号元素所在的位置,它为第七周期ⅣA族;${\;}_{114}^{298}$R的质子数为114,中子数为184,具有双幻数,${\;}_{114}^{289}$R的质子数为114,中子数为175,不具有双幻数,所以稳定性:${\;}_{114}^{298}$R>${\;}_{114}^{289}$R,故答案为:七;ⅣA;>.
点评 本题主要考查了晶体类型的判断、原子结构示意图、元素在周期表中的位置和利用信息解决问题的能力,难度不大,注意对信息的利用.


科目:高中化学 来源: 题型:选择题
| A. | $\frac{1}{3}$ | B. | $\frac{2}{3}$ | C. | $\frac{1}{2}$ | D. | $\frac{1}{6}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第四周期 | B. | 第二周期 | C. | 第ⅣA主族 | D. | 第ⅤA主族 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (一种常见化妆品的防霉剂),其生产过程如下图(反应条件没有全部注明):
(一种常见化妆品的防霉剂),其生产过程如下图(反应条件没有全部注明):
 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
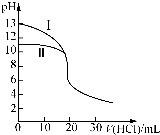 室温下,用0.10mol•L-1盐酸分别滴定20.00mL 0.10mol•L-1氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积[V(HCl)]的变化关系如图所示.下列说法不正确的是( )
室温下,用0.10mol•L-1盐酸分别滴定20.00mL 0.10mol•L-1氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积[V(HCl)]的变化关系如图所示.下列说法不正确的是( )| A. | Ⅱ表示的是滴定氨水的曲线,当V(HCl)=20 mL时,有:c(Cl-)>c(NH4+)>c(H+)>c(OH-) | |
| B. | 当pH=7时,滴定氨水消耗的V(HCl)=20 mL,且c(NH4+)=c(Cl-) | |
| C. | 滴定氢氧化钠溶液时,若V(HCl)>20 mL,则一定有:c(Cl-)>c(Na+)>c(OH-)>c(H+) | |
| D. | 当滴定氨水消耗V(HCl)=10 mL时,有:2[c(OH-)-c(H+)]=c(NH4+)-c(NH3•H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe和足量稀硝酸反应Fe+2H+═Fe2++H2↑ | |
| B. | 将Fe(NO3)3溶液与少量HI混合:8H++2NO3-+6I-═4H2O+3I2+2NO↑ | |
| C. | 用过量氨水吸收SO2的反应:NH3•H2O+SO2═NH4++HSO3- | |
| D. | 少量Ca(OH)2和NaHCO3反应 Ca2++OH-+HCO3-═CaCO3↓+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com