
某淡黄色的颗粒状固体,其化学性质比较活泼,在通常状况下能跟许多物质发生化学反应。例如:它与CO2反应时,只生成了Na2CO3和O2,它与稀盐酸反应时,只生成了NaCl、H2O和O2。上课时,老师做了如下实验:
a.取少量的淡黄色的颗粒状固体投入到盛有少量水的试管中,可观察到产生了一种无色无味的气体;
b.再向试管中滴加几滴酚酞试液,可观察到烧杯中溶液变红。
根据实验现象,回答下列问题:
(1)淡黄色的颗粒状固体中一定含有 元素。你做出这个判断的理由是 。
(2)实验a中产生的气体,可用 法收集。
(3)同学们对实验a中产生的气体的组成看法不一,提出了以下几种假设:
①该气体是CO; ②该气体是H2。
请你推测该气体还可能是 (写化学式)。
(4)设计一个实验,证明你在(3)中的推测(写出简要操作步 骤,反应现象和结论)。
骤,反应现象和结论)。
操作步骤 | |
反应现象 | |
结论 |
 口算能手系列答案
口算能手系列答案科目:高中化学 来源:2017届湖北省枣阳市高三上学期8月月考化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.可逆反应的特征是正反应速率和逆反应速率相等
B.在其他条件不变时,使用催化剂只能改变反应速率,而不能改变化学平衡状态
C.在其他条件不变时,升高温度可以使平衡向放热反应方向移动
D.在其他条件不变时,增大压强一定会破坏气体反应的平衡状态
查看答案和解析>>
科目:高中化学 来源:2017届广东省高三上8月月考化学试卷(解析版) 题型:填空题
(1)镁燃烧不能用CO2灭火,用化学方程式表示其理由 。
(2)用H2O2和稀H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜,请写出表示该过程的化学方程式 。
(3)在NaAlO2溶液中通入过量的CO2 (用离子方程式表示)
(4)污水及自来水处理的方法有很多。
Fe2(SO4)3 净水的原理是 。
使用时发现Fe2(SO4)3 并不能使酸性废水中的悬浮物沉降除去,其原因是 。
在酸性环境下,向含重铬酸根的废水中加入FeSO4溶液,然后调节pH,使生成的Cr3+转化为Cr(OH)3,写出第一步反应的离子方程式 。
(5)锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成Zn(NH3)42+,则下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是 。
①硫酸铝和氨水 ②偏铝酸钠和稀盐酸 ③ 硫酸锌和氢氧化钠 ④ 硫酸锌和氨水
查看答案和解析>>
科目:高中化学 来源:2016-2017年新疆兵团第二师华山中学高二上学前考化学卷(解析版) 题型:选择题
同周期的X、Y、Z三种元素,已知其最高价氧化物对应的水化物的酸性强弱顺序是:[HXO4>H2YO4>H3ZO4,则下列各判断中正确的是
A. 原子半径:X>Y>Z B. 单质的非金属性:X>Y>Z
C. 气态氢化物稳定性:X<Y<Z D. 原子序数:X<Y<Z
查看答案和解析>>
科目:高中化学 来源:2016-2017年新疆兵团第二师华山中学高二上学前考化学卷(解析版) 题型:选择题
标准状况下,0.56 L CH4和C2H4的混合气体通入足量溴水中,溴水增重0.28g,则乙烯占混合气体体积的百分比为
A.20% B.40% C.60% D.80%
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一上入学考化学试卷(解析版) 题型:实验题
小艾同学在妈妈买回的某食品包装内发现有一包白色颗粒状固体A的小纸袋,上面写着“生石灰干燥剂,请勿食用”。小艾同学随手将小纸袋放在窗台上,过一段时间后发现纸袋内的白色颗粒粘在一起成为块状固体B。小艾同学请你和同学们一起对块状固体B进行探究。
(1)猜想一:块状固体B中除氧化钙外,还可能有 (写两种);
(2)猜想二:块状固体B溶于水可能有 现象(填“放热”或“吸热”)。
(3)取块状固体B加入盛有一定量水的试管内,振荡、静置、过滤,得到少量白色固体C。就白色固体C同学们展开了热烈讨价,一起猜想。
小艾同学认为白色固体C可能是氢氧化钙,小聪同学认为白色固体C可能是碳酸钙;你认为白色固体C还可能是 (任写一种)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一上入学考化学试卷(解析版) 题型:选择题
“群众利益无小事,食品安全是大事”。下列作法不会导致食品对人体健康有害的是
A.用干冰保藏易变质的食品。
B.用硫磺熏制白木耳、粉丝等食品。
C.用甲醛浸泡易腐烂的食品。
D.用含亚硝酸钠的工业用盐腌制食品。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高一上开学考化学卷(解析版) 题型:选择题
化学实验中常涉及实验操作的先后顺序,下列实验操作不正确的是
A.制取二氧化碳时,先检查装置的气密性,后装药品
B.氢气还原氧化铜时,先通一会氢气,后加热氧化铜
C.给试管中的物质加热时,先均匀加热,后集中在药品的部位加热
D.用排水法收集氧气时,先撤酒精灯,后撤导气管
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上开学考化学试卷(解析版) 题型:填空题
碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
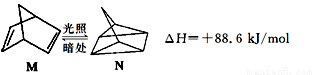
则M、N相比,较稳定的是 。
(2)已知CH3OH(l)的燃烧热为726.5kJ·mol-1,CH3OH(l) + 1/2O2(g) ═ CO2(g) + 2H2(g) △H=-a kJ·mol-1,则a 726.5(填“>”、“<”或“=”)。
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1mol Cl2参与反应时释放出145kJ热量,写出该反应的热化学方程式 。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)═2Al2O3(s)+3TiC(s) △H=-1176kJ·mol-1,则反应过程中,每转移1mol电子放出的热量为 。
(5)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H=+489.0 kJ·mol-1
CO(g)+1/2O2(g)=CO2(g) △H=-283.0kJ·mol-1
C(石墨)+O2(g)=CO2(g) △H=-393.5kJ·mol-1
则4Fe(s)+3O2(g)=2Fe2O3(s) △H= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com