
等物质的量的X(g)与Y(g)在密闭容器中进行反应:X(g)+2Y(g)3Z(g)+Q(s) △H >0,下列叙述正确的是:
A、当容器中X与Y的物质的量的比满足1:2时反应达到平衡
B、达到平衡时X的转化率为25%,则平衡常数K值为9/4
C、达到平衡后,反应速率2V正(Y)=3 V逆(Z)
D、达到平衡后,加入Q,平衡逆向移动
B
【解析】
试题分析:A、反应中X与Y按照1:2的物质的量比例进行反应,所以当容器中X与Y的物质的量的比满足1:2时反应不一定达到平衡,错误;B、设X、Y的起始物质的量都是1mol,达到平衡时X的物质的量是1mol×(1-25%)=0.75mol,消耗X的物质的量是0.25mol,则Y的物质的量是1mol-0.25mol×2=0.5mol,生成Z的物质的量是0.25mol×3=0.75mol,Q为固体,所以该反应是气体的物质的量不变的可逆反应,则平衡常数的计算可用物质的量代替,K=0.753/0.52×0.75=2.25=9/4,正确;C、达到平衡后,Z的逆反应速率是Y的正反应速率的3/2倍,则3V正(Y)=2 V逆(Z),错误;D、Q为固体,所以达平衡后,加入Q,平衡不移动,错误,答案选B。
考点:考查平衡常数的计算,平衡的判断与移动


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源:2014-2015湖南省娄底市高二上学期期末考试化学(理)试卷(解析版) 题型:填空题
(14分)在2L密闭容器内,800℃时反应2NO(g)+O2(g)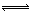 2NO2(g)体系中,n(NO)随时间变化如下表:
2NO2(g)体系中,n(NO)随时间变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K=__ __。已知:K(300℃)>K(350℃),则该反应正反应是__ _热反应。升高温度,正反应速率 (填“增大”、“减小”或“不变”)。
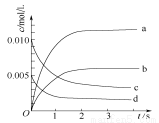
(2)下图中表示NO2的变化的曲线是____。用O2表示从0~2 s内该反应的平均速率v(O2)=______。
(3)能说明该反应已达到平衡状态的是__________。
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.v逆(NO)=2v正(O2) D.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是_________。
A.及时分离出NO2气体 B.适当升高温度 C.增大O2的浓度 D.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省茂名市高三一模考试理综化学试卷(解析版) 题型:选择题
在水溶液中能大量共存的一组离子是
A.Ag+、Ca2+、Cl-、Br- B.I-、H+、SO42-、 ClO-
C.Al3+、NH4+、Cl-、CO32- D.K+、Mg2+、NO3-、SCN-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省部分普高高三2月联考化学试卷(解析版) 题型:选择题
已知:
2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1
2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l) ΔH=-1452 kJ·mol-1
H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1
下列说法正确的是:
A.H2(g)的燃烧热为571.6 kJ·mol-1
B.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多
C.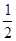 H2SO4(aq)+
H2SO4(aq)+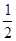 Ba(OH)2(aq)===
Ba(OH)2(aq)===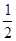 BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
D.3H2(g)+CO2(g)=CH3OH(l)+H2O(l) ΔH=+135.9 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省部分普高高三2月联考化学试卷(解析版) 题型:选择题
有五种饱和溶液①Ba(NO3)2 ②Ca(OH)2 ③NaAlO2 ④Na2CO3 ⑤NH3和NaCl,分别持续通入CO2,最终得到沉淀或析出晶体的是:
A.①②③④⑤ B.②③④⑤ C.③④⑤ D.③④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省福州市高三第六次月考理综化学试卷(解析版) 题型:实验题
(14分)工业上SnSO4是一种重要的硫酸盐,广泛应用于镀锡工业,其制备路线如下:

提示:①已知在酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式。
②已知Ksp[Sn(OH)2] =1.0×10-26
回答下列问题:
(1)SnCl2用盐酸而不用水直接溶解的原因是_____,加入Sn粉的作用是____。
(2)反应I生成的沉淀为SnO,写出该反应的离子方程式_______________。
(3)检验沉淀已经“漂洗”干净的方法__________________________。
(4)反应Ⅱ硫酸的作用之一是控制溶液的pH,若溶液中c(Sn2+)=1.0molL-1,则应控制溶液pH______。
(5)酸性条件下,SnSO4还可以用作双氧水去除剂,请写出发生反应的离子方程式________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省福州市高三第六次月考理综化学试卷(解析版) 题型:选择题
下列叙述中,正确的是
A.油脂是高分子化台物,水解可生成甘油和高级脂肪酸
B.葡萄糖注射液不能产生丁达尔效应,不属于胶体
C.煤中含有的煤焦油,可由煤干馏获得
D.聚乙烯塑料的老化是因为发生了加成反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三上学期期末考试化学试卷(解析版) 题型:选择题
室温时,0.1mo1/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是:
A.该溶液的pH=4
B.升高温度,溶液的pH增大
C.此酸的电离平衡常数约为1×10-7
D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com