
| A. | C(Na+)>C(Ac-)=C(OH-)>C(H+) | B. | C(Na+)>C(Ac-)>C(OH-)>C(H+) | ||
| C. | C(Na+)=C(Ac-)+C(HAc) | D. | C(Na+)+C(H+)=C(Ac-)+C(OH) |
分析 常温下,NaOH是强电解质、醋酸是弱电解质,pH=13的NaOH溶液浓度小于pH=1的醋酸溶液,在10mlpH=13NaOH溶液中加入PH=1的醋酸溶液,因为醋酸溶液体积未知,所以混合溶液中溶质可能是醋酸钠和NaOH,可能是醋酸钠,也可能是醋酸钠和醋酸,但无论溶液中溶质是什么,都遵循电荷守恒和物料守恒,据此分析解答.
解答 解:常温下,NaOH是强电解质、醋酸是弱电解质,pH=13的NaOH溶液浓度小于pH=1的醋酸溶液,在10mlpH=13NaOH溶液中加入PH=1的醋酸溶液,因为醋酸溶液体积未知,所以混合溶液中溶质可能是醋酸钠和NaOH,可能是醋酸钠,也可能是醋酸钠和醋酸,
A.如果溶液中溶质是醋酸钠和醋酸,且醋酸物质的量远远大于醋酸钠,则溶液呈酸性,溶液中存在C(OH-)<C(H+),故A错误;
B.如果溶液中溶质是醋酸钠,因为醋酸根离子水解而导致溶液呈碱性,则存在C(Na+)>C(Ac-)>C(OH-)>C(H+),如果溶液中溶质是醋酸和醋酸钠,且醋酸的物质的量远远大于醋酸钠,则溶液呈酸性,溶液中存在C(OH-)<C(H+),故B错误;
C.如果溶液中溶质为醋酸钠和醋酸,则存在C(Na+)<C(Ac-)+C(HAc),如果溶液中溶质为NaOH和醋酸钠,则存在C(Na+)>C(Ac-)+C(HAc),如果溶质为醋酸钠,则存在C(Na+)=C(Ac-)+C(HAc),故C错误;
D.无论溶液中溶质是什么,都存在电荷守恒,根据电荷守恒得C(Na+)+C(H+)=C(Ac-)+C(OH),故D正确;
故选D.
点评 本题考查离子浓度大小比较,为高频考点,侧重考查学生分析判断及发散思维能力,明确溶液中溶质成分及其性质是解本题关键,因为该题中醋酸溶液未知导致混合溶液中溶质成分未知,很多同学往往定性思维而导致错误,为易错题.


科目:高中化学 来源: 题型:多选题
| A. | 4FeS2( s)+11O2( g)═2Fe2O3( s)+8SO2(g)△H=-3414.8kJ•moL | |
| B. | FeS2(s)+$\frac{11}{4}$O2(g)═$\frac{1}{2}$Fe2O3 (s)+2SO2(g)△H=-853.7kJ•moL | |
| C. | 4FeS2(s)+11O2(g)═2 Fe2O3 (s)+8SO2(g)△H+3414.8kJ•moL | |
| D. | FeS2(s)+$\frac{11}{4}$O2(g)═$\frac{1}{2}$Fe2O3 (s)+2SO2(g)△H=+853.7kJ•moL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高压有利于氨的合成 | |
| B. | 向含有酚酞的氨水溶液中,加入少量NH4Cl晶体,溶液红色变浅 | |
| C. | 常温下,0.1 mol•L-1的盐酸中,由水产生的c(H+)<1.0×10-7mol•L-1 | |
| D. | 使用催化剂可加快SO2转化为SO3的反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 90mL容量瓶,7.2g | B. | 100mL容量瓶,8.0g | ||
| C. | 100mL容量瓶,7.2g | D. | 250mL容量瓶,20.0g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肥皂和合成洗涤剂的结构相似,都含有憎水基和亲水基 | |
| B. | 肥皂不适用于硬水中洗涤,合成洗涤剂可以 | |
| C. | 合成洗涤剂难以被微生物分解,所以去污能力比肥皂好 | |
| D. | 肥皂的生产原料是油脂,成本高,合成洗涤剂的生产原料是石油副产品,成本较低 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
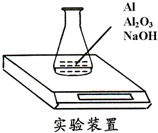 某种由Al与Al2O3粉末组成的混合物样品,利用如下图装置测定混合物中Al的质量分数(已知样品质量为2.58g、锥形瓶和过量NaOH溶液的总质量为185.72g),每隔相同时间读得电子天平的数据如下表:
某种由Al与Al2O3粉末组成的混合物样品,利用如下图装置测定混合物中Al的质量分数(已知样品质量为2.58g、锥形瓶和过量NaOH溶液的总质量为185.72g),每隔相同时间读得电子天平的数据如下表:| 读数次数 | 质量(g) | |
| 锥形瓶 + NaOH溶液 + 试样 | 第1次 | 188.30 |
| 第2次 | 188.28 | |
| 第3次 | 188.25 | |
| 第4次 | 188.24 | |
| 第5次 | 188.24 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com