
| 选项 | 实验事实 | 结论 |
| A | 二氧化硅可以和NaOH溶液及HF溶液反应 | 二氧化硅属于两性氧化物 |
| B | 二氧化硫能漂白有色布料 | 二氧化硫具有强氧化性 |
| C | 向饱和Na2CO3溶液中通入足量CO2,溶液变浑浊 | 析出了NaHCO3 |
| D | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝的熔点高 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.除HF外二氧化硅不与其它强酸反应,只属于酸性氧化物;
B.二氧化硫与有色物质结合生成不稳定的无色物质,其漂白性与强氧化性无关;
C.碳酸钠的溶解度大于碳酸氢钠;
D.氧化铝的熔点较高,加热过程中氧化铝包在铝外面,导致铝不会滴下.
解答 解:A.二氧化硅与NaOH溶液反应生成盐和水,不与HF以外的其它酸反应,则二氧化硅属于酸性氧化物,不属于两性氧化物,故A错误;
B.二氧化硫能够与有色物质结合转化成无色物质,导致二氧化硫具有漂白性,其漂白性与强氧化性无关,故B错误;
C.向饱和Na2CO3溶液中通入足量CO2,反应生成了溶解度较小的碳酸氢钠,从而有碳酸氢钠析出,溶液变浑浊,故C正确;
D.铝的熔点较低,而铝与氧气生成的氧化铝具有较高的熔点,导致加热熔化的铝不会滴下,故D错误;
故选C.
点评 本题考查了化学实验方案的评价,题目难度中等,涉及二氧化硅、二氧化硫、碳酸钠与碳酸氢钠、铝等性质及判断,明确常见元素及其化合物性质为解答关键,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 在相同条件下,1 mol H2(g)与0.5 mol O2(g)的能量总和大于1 mol H2O(g)的能量 | |
| B. | 标准状况下,1 mol H2(g)与0.5 mol O2(g)反应生成1 mol H2O放出的热量为241.8 kJ | |
| C. | 8 g水蒸气完全分解成氢气和氧气吸收483.6 kJ热量 | |
| D. | 常温下,2 mol H2与1 mol O2完全反应生成液态水放出的热量小于483.6 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
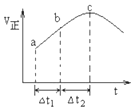 NO2与SO2混合可发生反应:NO2+SO2?SO3+NO.在100℃1molNO2与1molSO2的混合气体置于绝热(不与外界进行热交换)恒容密闭容器中发生上述反应,①正反应速率随时间变化的趋势如图所示,则下列说法正确的是C(填字母).
NO2与SO2混合可发生反应:NO2+SO2?SO3+NO.在100℃1molNO2与1molSO2的混合气体置于绝热(不与外界进行热交换)恒容密闭容器中发生上述反应,①正反应速率随时间变化的趋势如图所示,则下列说法正确的是C(填字母).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3 mol | B. | 1.5 mol | C. | 0.75 mol | D. | 0.6 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 2016年11月3日20点43分,中国首枚重型运载火箭“长征五号”在海南文昌航天发射场顺利点火升空.
2016年11月3日20点43分,中国首枚重型运载火箭“长征五号”在海南文昌航天发射场顺利点火升空.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com