
【题目】用钠熔法可定性确定有机物中是否存在氯、溴、硫、氮等元素。下列有关有机物与足量钠反应,各元素的转化结果正确的是
A. 碳元素转化为NaCN B. 氯元素转化为高氯酸钠
C. 溴元素转化为溴化钠 D. 硫元素转化为硫酸钠
科目:高中化学 来源: 题型:
【题目】某有机物在酸性条件下发生水解反应时,生成两种不同有机物,且这两种有机物的相对分子质量相等。则水解前的这种有机物是( )
A.甲酸甲酯B.乙酸异丙酯C.麦芽糖D.葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有反应N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0,
2NH3(g) ΔH<0,
(1)在恒温恒压条件下进行,反应正向进行的是________;反应逆向进行的是________;处于平衡状态的是________;无法判断是否达到平衡的是________。
A.单位时间内生成1mol N2,同时生成3mol NH3
B.单位时间内生成3mol N2,同时生成6mol N—H键
C.混合气体的密度不再随时间而改变
D.容器中气体的压强不再随时间而改变
(2)在一定温度下某恒容密闭容器中,充入3molH2和1mol的N2,2min达到平衡状态时,总的气体的物质的量变为原来的9/10,则此时N2的转化率为__________;
若此时放出的热量为18.44 kJ,则其热化学方程式为______________________________ .
根据所求出的热化学方程式,且已知1mol氮氮三键断裂需要为945.8kJ的能量,1mol氢氢键断裂需要436 kJ的能量,求1molN-H键断裂吸收的能量_____。
(3)氨气可用作碱性燃料电池的燃料,电池反应为4NH3+3O2═2N2+6H2O,
则氨燃料电池的负极电极反应为________________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组有机物,无论以何种物质的量的比例混合,只要总物质的量一定,则完全燃烧消耗氧气的量为一恒定值的是( )
A.C3H6和C3H8 B.C2H6和C2H4O2 C.C5H10和C6H6 D.C2H6和C3H8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学反应2 A![]() B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(molL-1)随反应时间(min)的变化情况如下表所示。
B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(molL-1)随反应时间(min)的变化情况如下表所示。
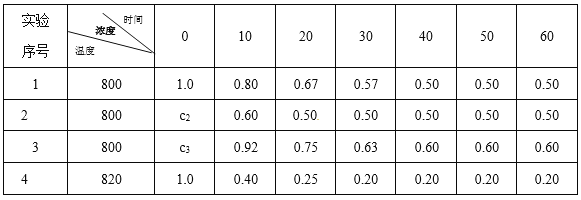
根据上述数据,完成下列填空:
(1)在实验1中,反应在10~20 min时间内A的平均反应速率为___________mol·L-1·min-1。
(2)在实验2中,A的初始浓度c2=________mol·L-1。
(3)设实验3的反应速率为v3。,实验1的反应速率为v1,则v3_____vl(填“>”、“="或“<”)。
(4)比较实验4和实验1,可推测该反应是_______(填“吸热”或“放热”)反应。
理由是_____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组对金牌成分提出猜想:甲认为金牌是由纯金制造;乙认为金牌是由金银合金制成;丙认为金牌是由黄铜(铜锌合金),为了验证他们的猜想,请你选择一种试剂来证明甲、乙、丙猜想的正误:
A.硫酸铜溶液 B.盐酸 C.稀硝酸 D.硝酸银溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G( ![]() )是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
)是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
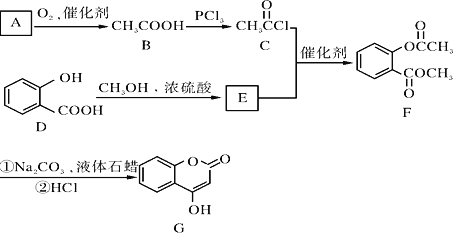
(1)A与银氨溶液反应有银镜生成,则A的结构简式是____________,D中官能团名称为_________________B→C的反应类型是________反应。
(2)下列关于G的说法不正确的是__________(填字母)。
A.能与溴的四氯化碳溶液反应 b.能与金属钠反应
C.1molG最多能和5mol氢气反应 d.分子式是C9H6O3
(3)写出满足下列条件的E的同分异构体的结构简式:___________________。
①苯环上的一氯取代产物只有一种;
②能发生银镜反应;
③能与FeCl3溶液发生显色反应。
(4)写出F和过量NaOH溶液共热时反应的化学方程式:_____________。
(5)请利用上述框图中的反应设计合理的方案,以苯酚和乙醇为原料合成乙酸苯酯![]() (用合成路线流程图表示,并注明反应条件).
(用合成路线流程图表示,并注明反应条件).
提示:①合成过程中无机试剂任选;②合成路线流程图示例如下:
CH3CH2OH![]() H2C=CH2
H2C=CH2![]() BrH2C-CH2Br.
BrH2C-CH2Br.
___________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电化学装置的叙述正确的是 ( )

A. 图1中,Zn—MnO2干电池放电时,MnO2被氧化
B. 图2中,电解精炼铜时,阳极减少的质量与阴极增加的质量一定相等
C. 图4中,在钢材上电镀铝,熔融盐中Al和Cl元素只以AlCl4-、Al2Cl7-形式存在,则阳极反应式为:Al -3e-+7AlCl4-=4Al2Cl7-
D. 图3中,K分别与M、N连接,均可保护Fe电极,连接M时称为“牺牲阳极的阴极保护法”
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com