
常温下测得某无色溶液中由水电离出的H+浓度为1×2013—13mol/L,又知该溶液中还有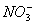 、Na+、
、Na+、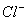 ,那么该溶液中还一定存在的离子是 ( )
,那么该溶液中还一定存在的离子是 ( )
A.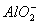 、
、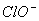 B.Mg2+、、
B.Mg2+、、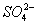 C.Fe2+ 、Cu2+ D.Ba2+、K+
C.Fe2+ 、Cu2+ D.Ba2+、K+
科目:高中化学 来源: 题型:
溶质质量分数为98%的浓硫酸(ρ=1.84g/mL),其物质的量浓度为18.4mol/L,取10mL该硫酸与amL水混合,配制成溶质质量分数为49%的硫酸(ρ=1.40g/mL),其物质的量浓度为b mol/L,则a、b分别为
A. a>10 b<9.2 B. a<10 b<9.2 C. a=10 b<9.2 D. a>10 b>9.2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中微粒的物质的量浓度关系正确的是( )
A.室温下,向0.1 mol·L-1NH4HSO4溶液中滴加等物质的量溶质的NaOH溶液:c(Na+)=c(SO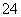 )>c(NH
)>c(NH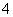 )>c(OH-)=c(H+)
)>c(OH-)=c(H+)
B.0.1 mol·L-1NaHCO3溶液:c(Na+)>c(OH-)>c(HCO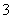 )>c(H+)
)>c(H+)
C.Na2CO3溶液:c(OH-)-c(H+)=c(HCO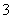 )+2c(H2CO3)
)+2c(H2CO3)
D.25℃时,pH=4.75,浓度均为0.1 mol·L-1的CH3COOH、CH3COONa混合溶液:c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)向NaHSO4溶液中,逐滴加入Ba(OH)2溶液中至中性,请写出发生反应的离子方程式: 。
(2)在以上中性溶液中,继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
若溶液中由水电离产生的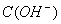 =1×2013—14mol·L-1,此溶液中一定可以大量共存的离子组是 ( )
=1×2013—14mol·L-1,此溶液中一定可以大量共存的离子组是 ( )
A. Al3+ 、Na+ 、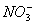 、
、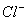 B. K+ 、Na+、
B. K+ 、Na+、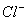 、
、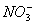
C. K+ 、Na+ 、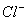 、
、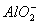 D. K+ 、 NH4+、
D. K+ 、 NH4+、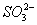 、
、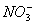
查看答案和解析>>
科目:高中化学 来源: 题型:
水体中重金属铅的污染问题备受关注。水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、Pb(OH)3-、Pb(OH)42-,各形态的浓度分数α随溶液pH变化的关系如图所示:
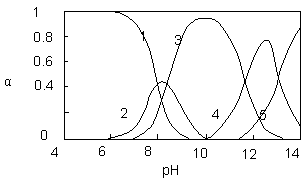
【1表示Pb2+,2表示Pb(OH)+,3表示Pb(OH)2,4表示Pb(OH)3-,5表示Pb(OH)42-】
⑴Pb(NO3)2溶液中,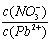 2 (填“>”、“=”、“<”);往该溶液中滴入氯化铵溶液后,
2 (填“>”、“=”、“<”);往该溶液中滴入氯化铵溶液后,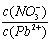 增加,可能的原因是 。
增加,可能的原因是 。
⑵往Pb(NO3)2溶液中滴稀NaOH溶液,pH=8时溶液中存在的阳离子(Na+除外)有
,pH=9时,主要反应的离子方程式为 。
⑶某课题组制备了一种新型脱铅剂,能有效去除水中的痕量铅,实验结果如下表:
 |
 离子 Pb2+ Ca2+ Fe3+ Mn2+ Cl-
离子 Pb2+ Ca2+ Fe3+ Mn2+ Cl-
处理前浓度/(mg·L-1) 0.20130 29.8 0.120 0.087 51.9
处理后浓度/(mg·L-1) 0.004 22.6 0.040 0.053 49.8
 上表中除Pb2+外,该脱铅剂对其它离子的去除效果最好的是 。
上表中除Pb2+外,该脱铅剂对其它离子的去除效果最好的是 。
⑷如果该脱铅剂(用EH表示)脱铅过程中主要发生的反应为:
2EH(s)+Pb2+ E2Pb(s)+2H+
E2Pb(s)+2H+
则脱铅的最合适pH范围为 (填代号)。
A.4~5 B.6~7 C.9~2013 D.2013~12
查看答案和解析>>
科目:高中化学 来源: 题型:
醋酸溶液中存在电离平衡:
CH3COOH H++CH3COO-,下列叙述不正确的是 ( )
H++CH3COO-,下列叙述不正确的是 ( )
A.醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-)
B.0.12mol/L的CH3COOH溶液加水稀释,溶液中c(OH-)减小
C.CH3COOH溶液中加入少量的CH3COONa固体,平衡逆向移动
D.常温下,pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列叙述中,能说明盐酸是强酸,醋酸是弱酸的是
A.将pH=4的盐酸和醋酸稀释成pH=5的溶液,醋酸所需加入的水量多
B.盐酸和醋酸都可用相应的钠盐与浓硫酸反应制取
C.相同pH值的盐酸和醋酸溶液中分别加入相应的钠盐固体,醋酸的pH值变化大
D.相同pH值的盐酸和醋酸分别跟锌反应时,产生氢气的起始速度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
某烃有两种或两种以上的同分异构体,其同分异构体中的某一种的一氯代物只有一种则这种烃可能是( )
①分子中具有7个碳原子的芳香烃 ②分子中具有4个碳原子的烷烃 ③分子中具有12个氢原子的烷烃 ④分子中具有6个碳原子的烷烃 ⑤分子中具有8个碳原子的烷烃
A. ①②③ B. ③⑤ C. ③④⑤ D. ②③④⑤
Ⅱ(8分)有机物A由碳、氢、氧三种元素组成。现取2.3 g A与2.8 L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余)。将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重2.7 g,碱石灰增重2.2 g。回答下列问题:
(1)2.3 g A中所含氢原子、碳原子的物质的量各是多少?
(2)通过计算确定该有机物的分子式;
(3)试写出该有机物可能的结构简式.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com