
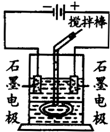
 在玻璃圆筒中盛有两种无色的互不相溶的中性液体.上层液体中插入两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅拌棒,可以上下搅动液体,装置如图.接通电源,阳极周围的液体呈现棕色,且颜色由浅变深,阴极上有气泡生成.停止通电,取出电极,用搅拌棒上下剧烈搅动.静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色.
在玻璃圆筒中盛有两种无色的互不相溶的中性液体.上层液体中插入两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅拌棒,可以上下搅动液体,装置如图.接通电源,阳极周围的液体呈现棕色,且颜色由浅变深,阴极上有气泡生成.停止通电,取出电极,用搅拌棒上下剧烈搅动.静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色.

 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
| A、强电解质溶液的导电能力一定比弱电解质强 |
| B、相同温度下,0.1mol?L-1 NH4Cl溶液中NH4+的浓度比0.1mol?L-1氨水中NH4+的浓度大 |
| C、盐酸中加入固体NaCl,因Cl-浓度增大,所以溶液酸性减弱 |
| D、冰醋酸是弱电解质,液态时能导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
35 17 |
37 17 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
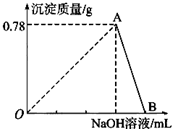 向20mL AlCl3溶液中滴入2mol?L-1NaOH溶液时,沉淀质量与所滴加NaOH溶液体积(mL)关系如图所示:
向20mL AlCl3溶液中滴入2mol?L-1NaOH溶液时,沉淀质量与所滴加NaOH溶液体积(mL)关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
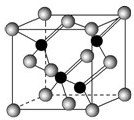 Ⅰ.2010年上海世博会场馆,大量的照明材料或屏幕都使用了发光二极管(LED).目前市售LED品片,材质基本以GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、InGaN(氮化铟镓)为主.已知镓是铝同族下一周期的元素.砷化镓的晶胞结构如右图所示.试回答:
Ⅰ.2010年上海世博会场馆,大量的照明材料或屏幕都使用了发光二极管(LED).目前市售LED品片,材质基本以GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、InGaN(氮化铟镓)为主.已知镓是铝同族下一周期的元素.砷化镓的晶胞结构如右图所示.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氨气通入水中能得NH3?H2O |
| B、四氯化碳萃取碘水中的碘 |
| C、过滤除去粗盐中的不溶性杂质 |
| D、蒸馏法将海水淡化为饮用水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com