
【题目】如图所示,左室容积为右室的两倍,温度相同,现分别按照如图所示的量充入气体,同时加入少量固体催化剂使两室内气体充分反应达到平衡,打开活塞,继续反应再次达到平衡,下列说法不正确的是( )

A. 第一次平衡时,SO2的物质的量左室更多
B. 入气体未反应前,左室压强和右室样大
C. 第一次平衡时,左室内压强一定小于右室
D. 第二次平衡时,SO2的总物质的量比第一次平衡时左室SO2的物质的量的2倍还要多
【答案】D
【解析】由于为恒容容器,1molAr对化学平衡无影响,容器中发生的反应为2SO2(g)+O2(g)![]() 2SO3(g)。A项,若右室的容积与左室相等,左室和右室在相同条件达到的平衡状态相同,含有的SO2物质的量相等,右室在此平衡时将体积缩小为1/2,增大压强,平衡向正反应方向移动,SO2物质的量减少,第一次平衡时,SO2物质的量左室更多,A项正确;B项,通入气体未反应前,左室气体总物质的量为2mol+1mol+1mol=4mol,右室气体总物质的量为2mol,左室容积为右室的两倍,温度相同,则左室压强和右室一样大,B项正确;C项,左室从正反应开始建立平衡,左室平衡时压强小于左室起始压强,右室从逆反应开始建立平衡,右室平衡时压强大于右室起始时压强,左室与右室起始压强相等,则第一次平衡时左室内压强一定小于右室,C项正确;D,若在容积为2倍左室容积的容器中起始充入4molSO2、2molO2,相同条件下达到平衡时SO2物质的量为左室SO2物质的量的2倍,打开活塞相当于容积为1.5倍左室容积的容器中起始充入2molSO2、1molO2、2molSO3(g)、1molAr,等效于容积为1.5倍左室容积的容器中起始充入4molSO2、2molO2、1molAr,相对于2倍左室容积的容器缩小体积,增大压强,平衡向正反应方向移动,SO2物质的量减小,即第二次平衡时,SO2的总物质的量比第一次平衡时左室SO2物质的量的2倍要少,D项错误;答案选D。
2SO3(g)。A项,若右室的容积与左室相等,左室和右室在相同条件达到的平衡状态相同,含有的SO2物质的量相等,右室在此平衡时将体积缩小为1/2,增大压强,平衡向正反应方向移动,SO2物质的量减少,第一次平衡时,SO2物质的量左室更多,A项正确;B项,通入气体未反应前,左室气体总物质的量为2mol+1mol+1mol=4mol,右室气体总物质的量为2mol,左室容积为右室的两倍,温度相同,则左室压强和右室一样大,B项正确;C项,左室从正反应开始建立平衡,左室平衡时压强小于左室起始压强,右室从逆反应开始建立平衡,右室平衡时压强大于右室起始时压强,左室与右室起始压强相等,则第一次平衡时左室内压强一定小于右室,C项正确;D,若在容积为2倍左室容积的容器中起始充入4molSO2、2molO2,相同条件下达到平衡时SO2物质的量为左室SO2物质的量的2倍,打开活塞相当于容积为1.5倍左室容积的容器中起始充入2molSO2、1molO2、2molSO3(g)、1molAr,等效于容积为1.5倍左室容积的容器中起始充入4molSO2、2molO2、1molAr,相对于2倍左室容积的容器缩小体积,增大压强,平衡向正反应方向移动,SO2物质的量减小,即第二次平衡时,SO2的总物质的量比第一次平衡时左室SO2物质的量的2倍要少,D项错误;答案选D。


科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+ 5O2(g)![]() 4NO(g)+ 6H2O(g),下列叙述正确的是
4NO(g)+ 6H2O(g),下列叙述正确的是
A. 达到化学平衡时,4υ正(O2)= 5υ逆(NO)
B. 若单位时间内生成x mol NO的同时,消耗x mol NH3 ,则反应达到平衡状态
C. 达到化学平衡时,若增加容器体积,则正反应速率减少,逆反应速率增大
D. 化学反应速率关系是:2υ正(NH3)= 3υ正(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃的混和物共0.1mol,完全燃烧后得3.36L(标况下)CO2和3.6g水,下列说法正确的是( )
A. 一定有乙烯B. 一定有甲烷
C. 可能有乙烷D. 一定有乙烷,但不一定有甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知液氨的性质与水相似。T℃时,NH3+NH3![]() NH4++NH2-,NH4+的平衡浓度为1×10-15mol/L,则下列说法中正确的是( )
NH4++NH2-,NH4+的平衡浓度为1×10-15mol/L,则下列说法中正确的是( )
A. 在此温度下液氨的离子积为1×10-17
B. 在液氨中放入金属钠,可生成NaNH2
C. 恒温下,在液氨中加入NH4Cl,可使液氨的离子积减小
D. 降温,可使液氨电离平衡逆向移动,且c(NH4+)<c(NH2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】糖尿病是由于人体内胰岛素紊乱导致的代谢紊乱综合征,以高血糖为主要标志。长期摄入高热量食品或缺少运动,都会导致糖尿病。
(1)血糖是指血液中的葡萄糖,下列有关说法正确的是______________。
A.葡萄糖分子可表示为C6(H2O)6,则每个葡萄糖分子含有6个H2O分子
B.葡萄糖与果糖互为同分异构体
C.糖尿病人尿糖较高,可用新制的氢氧化铜来检测人尿液中的葡萄糖
D.淀粉水解的最终产物是氨基酸
(2)糖尿病人不可过量饮酒,将会一定程度上造成胰岛细胞损伤。但酒精在肝脏内可转化成有机物A。A的实验结果如下:
①通过实验测得A的相对分子质量为60;
②A由C、H、O三种元素组成,分子中只存在两种类型的氢原子,且这两种类型的氢原子个数比为1∶3
③A可与酒精在一定条件下生成有芳香气味的物质。
纯净的A又称为______________,结构简式为____________________。
A的主要化学性质有(用化学方程式表示):a____________________________________,
b___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于共价键的说法正确的是( )
A.丙炔分子中含有5个σ键和2个π键
B.乙醇分子中O-H键的极性强于C-H键的极性
C.乙烷分子中只含有极性键不含有非极性键
D.分子晶体中共价键键能越大,该分子晶体的熔点和沸点一定也越高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外实验小组设计的下列实验不合理的是( )
A. 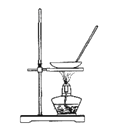 蒸干NH4Cl饱和溶液制备NH4Cl晶体
蒸干NH4Cl饱和溶液制备NH4Cl晶体
B. 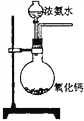 实验室制备少量氨气
实验室制备少量氨气
C. 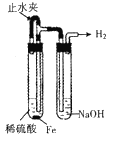 制备并观察氢氧化亚铁
制备并观察氢氧化亚铁
D. 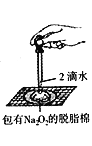 证明过氧化钠与水反应放热
证明过氧化钠与水反应放热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某课外活动小组同学用如图装置进行实验,试回答下列问题:
①若开始时开关K与a连接,则铁发生电化学腐蚀中的________腐蚀。
②若开始时开关K与b连接,则总反应的离子方程式为____________________________。
(2)芒硝化学式为Na2SO4·10H2O,无色晶体,易溶于水,是一种分布很广泛的硫酸盐矿物。该小组同学设想,如果模拟工业上离子交换膜法制烧碱的方法,用如图所示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧化钠,无论从节省能源还是从提高原料的利用率而言都更加符合绿色化学理念。
①该电解槽的阳极反应式为______________________________________。
此时通过阴离子交换膜的离子数________(填“大于”、“小于”或“等于”)通过阳离子交换膜的离子数
②制得的氢氧化钠溶液从出口(填写“A”、“B”、“C”或“D”)________导出。

③通电开始后,阴极附近溶液pH会增大,请简述原因:____________________________。
④若将制得的氢气、氧气和氢氧化钠溶液组合为氢氧燃料电池,则电池负极的电极反应式为______________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com