
��14�֣�Ϊ�˼���úȼ�նԴ�����ɵ���Ⱦ��ú��������Һ���Ǹ�Ч���������ú̿����Ҫ;����������CO2������ŷ�Ҳ���������ٵ��ش���⣮ú�ۺ����õ�һ��;��������ʾ��
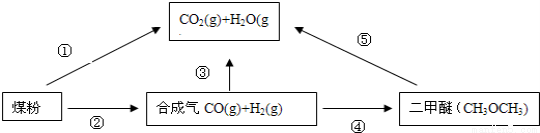
��1����֪��C(s)+H2O(g)====CO(g)+H2(g) ��H1=+131.3kJ?mol-1
C(s)+2H2O(g)====CO2(g)+2H2(g) ��H2=+90kJ?mol-1
��һ����̼��ˮ������Ӧ���ɶ�����̼���������Ȼ�ѧ����ʽ�� ��
��2����ȼú�����е�CO2ת��Ϊ�����ѵķ�Ӧԭ��Ϊ��2CO2(g)+6H2(g)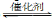 CH3OCH3(g)+3H2O(g)����H
CH3OCH3(g)+3H2O(g)����H
�ٸ÷�Ӧƽ�ⳣ������ʽΪK�� ��
����֪��ijѹǿ�£��÷�Ӧ�ڲ�ͬ�¶ȡ���ͬͶ�ϱ�ʱ��CO2��ת������ͼ��ʾ��
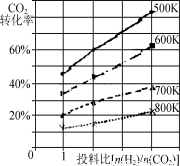
�÷�Ӧ�Ħ�H________(�>������<������)0�����¶Ȳ��䣬��С��ӦͶ�ϱ�[n(H2) /n(CO2)]����K��________(���������С�����䡱)��
��3��һ����������ȼ�ϵ�ع���ԭ������ͼ��ʾ��
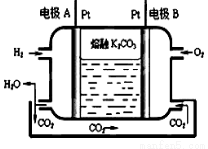
��д���缫A�ĵ缫��Ӧʽ �ŵ�����У���Һ�е�CO32-������缫 ����A��B��
����������ص�ⱥ��ʳ��ˮ��������0.2mol Cl2����������ͨ��O2�����Ϊ L����״����
��ÿ��2�֣���14�֣�
��1��CO(g)+H2O(g)====CO2(g)+H2(g) ��H=-41.3kJ?mol-1��
��2���� c(CH3OCH3)��c3(H2O)]/[c2(CO2)��c6(H2) �� < ����
��3����H2-2e-+CO32-= CO2+ H2O��A
��2.24
��������
�����������1�����ݸ�˹���ɵã�һ����̼��ˮ������Ӧ���ɶ�����̼���������Ȼ�ѧ����ʽΪCO(g)+H2O(g)====CO2(g)+H2(g) ��H=��H2-��H1=+90kJ?mol-1-131.3kJ?mol-1=-41.3kJ?mol-1��
��2���ٸ���ƽ�ⳣ���Ķ��壬�÷�Ӧ��ƽ�ⳣ��K= c(CH3OCH3)��c3(H2O)]/[c2(CO2)��c6(H2)��
�ڸ���ͼ���֪�����¶����ߣ�������̼��ת���ʽ��ͣ�˵�������¶ȣ�ƽ�������ƶ�����������Ӧ�Ƿ��ȷ�Ӧ����H<0��ƽ�ⳣ��ֻ���¶��йأ����¶Ȳ��䣬 ��С��ӦͶ�ϱ�[n(H2) /n(CO2)]����K�����䣻
��3���ٵ缫Aͨ������������������Ӧ������A�Ǹ���������ʧȥ���ӣ���̼������ӽ��Ϊˮ�Ͷ�����̼���壬�缫��ӦʽΪ��H2-2e-+CO32-= CO2+ H2O��ԭ����У����������ƶ�����̼���������A���ƶ���
������0.2mol Cl2����ת��0.4mol���ӣ�����O2+4e-+2CO2=2CO32-������Ҫ���������ʵ�����0.1mol����״���µ������0.1mol��22.4L/mol=2.24L��
���㣺�����˹���ɵ�Ӧ�ã�ƽ�ⳣ���ı�ʾ���жϣ�ԭ��ط�Ӧԭ����Ӧ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ����У�����ڶ���������ѧ�Ծ��������棩 ���ͣ�ѡ����
��������ѧ��ѧ�Ҳ��á����ת������������������̼��һ��������ת��Ϊ��Ҫ�Ļ���ԭ����ϩ��2CO2(g)+6H2(g)  C2H4(g)+4H2O(g)����H��+1411.0 kJ/mol,���ڸ÷�Ӧ������ͼʾ���Ӧ�������������
C2H4(g)+4H2O(g)����H��+1411.0 kJ/mol,���ڸ÷�Ӧ������ͼʾ���Ӧ�������������
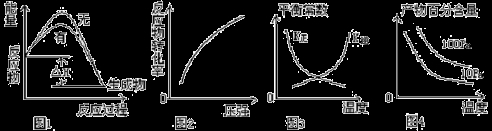
A��ͼ1��ʾ�÷�Ӧ�ֱ����С�����������·�Ӧ�����е������仯
B��ͼ2��ʾһ�������·�Ӧ�ﵽƽ���ı�ѹǿ��Ӧ���ת���ʵı仯
C��ͼ3��ʾһ�������·�Ӧ�ﵽƽ���ı��¶ȷ�Ӧƽ�ⳣ���ı仯
D��ͼ4 ��ʾһ�������·�Ӧ�ﵽƽ���ı��¶ȡ�ѹǿ����ٷֺ����ı仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ�����и�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ƶ���ȷ����
A��SiO2����NaOH��Һ��HF��Һ��Ӧ������SiO2������������
B��Na2O��Na2O2���Ԫ����ͬ���������������Ӹ�����Ҳ��ͬ
C��CO��NO��NO2���Ǵ�����Ⱦ���壬�ڿ����ж����ȶ�����
D��������ˮ�����ԣ������еμ�������ɫʯ����Һ���������Һ�ʺ�ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ����1�¼�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ƶ���ȷ����
A��SiO2 ���������������NaOH��Һ��Ӧ
B��Na2O��Na2O2���Ԫ����ͬ���� CO2��Ӧ����Ҳ��ͬ
C��CO��NO��NO2���Ǵ�����Ⱦ���壬�ڿ����ж����ȶ�����
D��������ˮ�����ԣ������еμ�������ɫʯ����Һ���������Һ�ʺ�ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ����1�¼�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
ij���ʵ�ˮ��Һ�ܵ��磬�Ҹ��������ڷǵ���ʣ�����ˮ��ѧ�����ƻ�����
A��Һ�� B���ɱ� C������ D�����ᱵ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ����12��ѧ����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��һ���¶��£�������X������Y��0.16mol���� 10L�����ܱ������У�������Ӧ
X(g) + Y(g)  2Z(g) ��H < 0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
2Z(g) ��H < 0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
t /min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
����˵����ȷ����
A����Ӧǰ2min��ƽ������v(Z) =4.0��10-3mol/(L?min)
B�������������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ǰv(��) > v(��)
C�����¶��´˷�Ӧ��ƽ�ⳣ��K=1.44
D�������������䣬�ٳ���0.2molZ��ƽ��ʱX�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ����12��ѧ����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ʵ�ת���ڸ�����������ʵ�ֵ���
��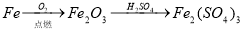
��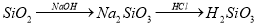
��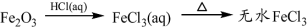
��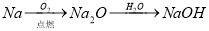
��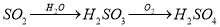
A���٢� B���ڢ� C���ۢ� D���ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ�����и�����ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���л�ѧʵ����ʵ������ͻ���۶���ȷ����
A��ȡ������ҺX�������м�������������ˮ���ټӼ���KSCN��Һ����Һ��죬˵��X��Һ��һ������Fe2����
B��ȡ����±����Y�ڼ�����Һ��ˮ������������ữ���ٵμ�AgNO3��Һ�����ɰ�ɫ������˵��±�����к�����ԭ�ӡ�
C����1 mL 1����NaOH��Һ�м���2 mL 2%��CuSO4��Һ�����ټ���0.5 mL�л���Y�����Ⱥ�δ����ש��ɫ������˵��Y�в�����ȩ����
D����Ũ�Ⱦ�Ϊ0.1 mol��L��1��MgCl2��CuCl2�����Һ����μ��백ˮ����������ɫ������˵��Ksp[Cu(OH)2]��Ksp[Mg(OH)2]��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2015����ʡ�߶�12��ѧ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪�¶�Tʱˮ�����ӻ�����Ϊ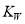 �����¶��£���Ũ��Ϊamol/L��һԪ��HA��b mol/L��һԪ��BOH�������ϣ����ж�����Һ�����Ե�������
�����¶��£���Ũ��Ϊamol/L��һԪ��HA��b mol/L��һԪ��BOH�������ϣ����ж�����Һ�����Ե�������
A��a=b
B�������Һ��pH=7
C�������Һ�У�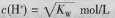
D�������Һ�У�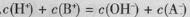
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com