
| A. | A的转化率变小 | B. | 平衡向逆反应方向移动 | ||
| C. | D的体积分数变大 | D. | a+b>c+d |
分析 将气体体积压缩到原来的一半,若平衡不移动,则D的浓度为原平衡浓度的2倍,而当再次达到平衡时,D的浓度为原平衡浓度的1.2倍,可知压强增大,平衡逆向移动,以此来解答.
解答 解:由信息可知,将气体体积压缩到原来的一半,若平衡不移动,则D的浓度为原平衡浓度的2倍,而当再次达到平衡时,D的浓度为原平衡浓度的1.2倍,可知压强增大,平衡逆向移动,则
A.平衡逆向移动,A的转化率变小,故A正确;
B.由上述分析可知,平衡向逆反应方向移动,故B正确;
C.平衡逆向移动,D的体积分数减小,故C错误;
D.加压平衡逆向移动,则a+b<c+d,故D错误;
故选AB.
点评 本题考查化学平衡的影响因素,为高频考点,把握D浓度的变化判断平衡移动的方向为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:选择题
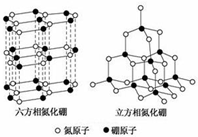 氮化硼(BN)晶体有多种相结构.六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂,但不能导电.立方相氮化硼是超硬材料,有优异的耐磨性.它们的晶体结构如图所示.关于这两种晶体的说法,正确的是( )
氮化硼(BN)晶体有多种相结构.六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂,但不能导电.立方相氮化硼是超硬材料,有优异的耐磨性.它们的晶体结构如图所示.关于这两种晶体的说法,正确的是( )| A. | 立方相氮化硼含配位键B→N | |
| B. | 六方相氮化硼层间作用力小,所以质地软,熔点低 | |
| C. | 两种氮化硼中的硼原子都是采用sp2杂化 | |
| D. | 六方相氮化硼晶体其结构与石墨相似却不导电,原因是没有可以自由移动的电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
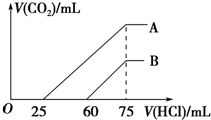 向浓度相等、体积均为50mL的A、B两份NaOH溶液中,分别通入一定量的CO2后,再稀释到100mL.在稀释后的溶液中逐滴加入0.1mol.L-1的盐酸,产生CO2的体积(标准状况)与所加盐酸的体积关系如图所示.下列说法正确的是( )
向浓度相等、体积均为50mL的A、B两份NaOH溶液中,分别通入一定量的CO2后,再稀释到100mL.在稀释后的溶液中逐滴加入0.1mol.L-1的盐酸,产生CO2的体积(标准状况)与所加盐酸的体积关系如图所示.下列说法正确的是( )| A. | 在NaOH溶液中通入一定量的CO2后,溶液中溶质的组成可能是①NaOH、Na2CO3 ②Na2CO3③Na2CO3、NaHCO3 ④NaHCO3 | |
| B. | B曲线说明,原溶液通入CO2后,所得溶质与盐酸反应产生CO2的最大体积是11.2L(标准状况) | |
| C. | 原NaOH溶液的物质的量浓度为0.100mol/L | |
| D. | B曲线表明,原溶液通入CO2后,所得溶液中溶质的化学式为NaOH、Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5min内平均反应速率vA=0.15mol•L-1•min-1 | |
| B. | 当同时对原平衡体系升高一定温度和增加一定压强时,达平衡后,C的物质的量分数为60%,则该反应的正反应为吸热反应 | |
| C. | 保持其他条件不变,若起始时向容器中加入0.5molA、0.5molB、1.5molC,则反应将向逆反应方向进行 | |
| D. | t℃,向2L密闭、恒容容器中仍充入1molA和1molB,反应达到平衡状态时,C的物质的量分数小于60% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .某油田开采的石油中溶有一种碳氢化合物--金刚烷,它的分子立体结构如图所示:
.某油田开采的石油中溶有一种碳氢化合物--金刚烷,它的分子立体结构如图所示:
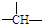 ”结构.
”结构.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知反应:2SO2(g)+O2(g)?2SO3(g)△H<0.一定温度下,在容积为2L的甲、乙、丙三个恒温密闭容器中,充入的SO2(g)和O2(g)的量如图所示:
已知反应:2SO2(g)+O2(g)?2SO3(g)△H<0.一定温度下,在容积为2L的甲、乙、丙三个恒温密闭容器中,充入的SO2(g)和O2(g)的量如图所示:| A. | 三个容器中的反应速率相同 | |
| B. | 丙中的平衡常数最大,甲中最小 | |
| C. | 当容器甲中SO2的转化率为80%时,该反应的平衡常数为160 | |
| D. | 达到平衡时,容器丙中的c(SO3)是容器甲中的两倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18gH2O中含有的质子数为10NA | |
| B. | 常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2NA | |
| C. | 46g NO2和N2O4混合气体中含有原子总数为3NA | |
| D. | 1molNa与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NA个氧气分子的体积约为11.2L | |
| B. | 1.8g的NH4+离子中含有的电子数为10NA | |
| C. | 标准状况下,2.24 L氢气和氧气以任意比组成的混合气体,所含的原子数约为0.2NA | |
| D. | 7.8g过氧化钠固体中含有的阴、阳离子的总数约为0.4 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com