
| A.NH3 | B.BCl3 | C.PCl3 | D.H2O |
科目:高中化学 来源:不详 题型:单选题
| A.乙烯的结构简式为:CH2CH2 |
| B.苯的分子式为:C6H6 |
C.Cl-的结构示意图为: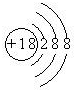 |
D.NaCl的电子式: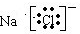 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CS2是V形分子 | B.SnBr2键角大于120° |
| C.BF3是三角锥形分子 | D.NH4+键角等于109.5° |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.化学键都具有饱和性和方向性 |
| B.晶体中只要有阴离子,就一定有阳离子 |
| C.氢键具有方向性和饱和性,也属于一种化学键 |
| D.金属键由于无法描述其键长、键角,故不属于化学键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验事实 | 理论解释 |
| A | 氮原子的第一电离能大于氧原子 | 氮原子2p能级半充满 |
| B | CO2为直线形分子 | CO2分子中C—O是极性键 |
| C | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是原子晶体 |
| D | HF的沸点高于HCl | HF的相对分子质量小于HCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com