
����Ŀ���ڻ�ѧ��Ӧ�У�ֻ�м�����������ƽ�������ߵö�ķ�Ӧ����ӷ� ����ײʱ�ſ��ܷ�����ѧ��Ӧ����Щ���ӱ���Ϊ����ӡ�ʹ��ͨ���ӱ�ɻ���������ṩ������ȵ������л�ܣ��䵥λͨ���� kJ/mol ��ʾ��������۲���ͼ��Ȼ�� �ش����⡣

��1��ͼ����ʾ��Ӧ��_____(����ȡ����ȡ�)��Ӧ��
��2����֪�� 1mol H��H ����1mol I��I��1mol H��I ���ֱ���Ҫ���յ�����Ϊ 436kJ��151kJ��299kJ������ 1mol ������ 1mol �ⷴӦ���� HI ��_____(��ų������� �ա�)______kJ ���������ڻ�ѧ��Ӧ�����У��ǽ�_____ת��Ϊ_________��
��3�����з�Ӧ�У����ڷ��ȷ�Ӧ����_____���������ȷ�Ӧ����_____��
������ȼ�� ��ըҩ��ը ������кͷ�Ӧ �ܶ�����̼ͨ�����ȵ�̼
��ʳ�������������� ��Ba(OH)2��8H2O �� NH4Cl ��Ӧ ��������ϡ���ᷴӦ
���𰸡� ���� �ų� 11 ��ѧ�� ���� �٢ڢۢݢ� �ܢ�
��������(1)����ͼ�������Ӧ��������������������������Ӧ���ȣ��ʴ�Ϊ�����ȣ�
(2)�ڷ�ӦH2+I2![]() 2HI�У�����1molH-H����1molI-I�������յ�����Ϊ��1��436kJ+151kJ=587kJ������2molHI�����γ�2molH-I�����ų�������Ϊ��2��299kJ=598kJ�����յ������٣��ų��������࣬���Ը÷�ӦΪ���ȷ�Ӧ���ų�������Ϊ��598kJ-587kJ=11kJ����ѧ��ת��Ϊ���ܣ��ʴ�Ϊ���ų���11����ѧ�ܣ����ܣ�
2HI�У�����1molH-H����1molI-I�������յ�����Ϊ��1��436kJ+151kJ=587kJ������2molHI�����γ�2molH-I�����ų�������Ϊ��2��299kJ=598kJ�����յ������٣��ų��������࣬���Ը÷�ӦΪ���ȷ�Ӧ���ų�������Ϊ��598kJ-587kJ=11kJ����ѧ��ת��Ϊ���ܣ��ʴ�Ϊ���ų���11����ѧ�ܣ����ܣ�
(3)�����ķ��ȷ�Ӧ�У����е�����ȼ�ա����н������ᷴӦ��������ˮ��Ӧ�������кͷ�Ӧ������������Ϸ�Ӧ�����ȷ�Ӧ�����������ȷ�Ӧ�У��������ֽⷴӦ������Ļ��Ϸ�Ӧ(��C��CO2)��ijЩ���ֽ�(����κ�ǿ��)�����Է��ȷ�Ӧ�У��٢ڢۢݢߣ����ȷ�Ӧ�У��ܢޣ��ʴ�Ϊ���٢ڢۢݢ����ܢ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£����ݻ�Ϊ2L���ܱ�������ͨ���������巢����ѧ��Ӧ����Ӧ�и����ʣ�A��B��C��D�������ʵ����仯��ͼM��ʾ���Ը÷�Ӧ���ƶϺ������ǣ������� 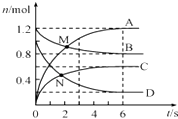
A.M���ʾv��A��=v��B��
B.0��6s�ڣ�v��A����v��B����v��C����v��D��=3��1��1.5��2
C.��Ӧ���е�6sʱ�������ʵ����ʵ���Ũ�����
D.��Ӧ���е�6sʱ��C��ƽ����Ӧ����Ϊ 0.1molL��1s��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ũ�Ⱦ�Ϊ0.1molL��1��������Һ�� ��Na2CO3��NaHCO3��HCl ��NH3H2O
��1�����˳���Һ�������۵ġ������ԭ�����������ӷ���ʽ���ͣ�
��2����������Һ��ˮ�ĵ���̶��ɴ�С��˳���ǣ��������д��
��3������м��������Ȼ�粒��壬��ʱ ![]() ��ֵ���������С�����䡱����
��ֵ���������С�����䡱����
��4���������Ϣۺܵ͢���Һ����ʱ��Һ��[NH4+]+[NH3H2O]=molL��1������ֵ������ʱ��Һ������Ũ�ȵĴ�С˳���ǣ��������ۺܵ͢���Һ��Ϻ���Һǡ�ó����ԣ�����ǰ�۵�����ܵ����������ڡ�С�ڡ����ڡ���
��5����10mL��Һ�ۼ�ˮϡ����100mL�����ʱ��Һ����ˮ�������c�� H+��= molL��1 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʹ����¯���ȣ�����ʹ�������ʾ������ȡ�����һ�¡��ٶȿ졢��Ч�ʸߵ��ŵ㡣�乤��ԭ����ͨ���¯�ڵ������Լ��ں��ȵĸ�Ƶ�ı���糡�ķ���ˮ���������Ѹ�ٰڶ���������ЧӦ��������Ϊ(����)
A. ˮ���Ӿ��м��Թ��ۼ� B. ˮ�����Ǽ��Է���
C. ˮ���⡢����Ԫ����� D. ˮ�������й��õ��Ӷ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�ػ��ϼ����ߣ�������Ԫ�ص�ԭ����_____�����ӣ�����Ԫ�ص����ʷ�����_____����Ӧ��������������_____������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ���۵�ߡ�Ӳ�ȴ����ԵĽ������㷺Ӧ���ڸ��������պ��졢��Դ������������Ŀǰ��ҵ��ʹ��һ���¹��գ��Ա��ұ�����Ĺ������һ��������ȡ��������������Ҫ����Fe2O3��Al2O3��V2O5��CuO�����幤������ͼ����:
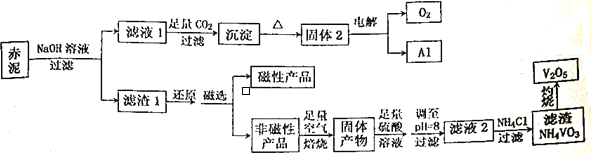
��֪:���ж��ּ�̬������+5�����ȶ���������Һ����Ҫ��VO2+��VO3-����ʽ���ڣ��Ҵ���ƽ��VO2++H2O![]() VO3-+2H+���ش���������:
VO3-+2H+���ش���������:
(1)���Բ�Ʒ�Ļ�ѧʽΪ_________________________��
(2)�������NaOH��Һ�����������ӷ�Ӧ����ʽΪ___________________���ܷ��ð�ˮ����NaOH��Һ��___________(��ܡ����ܡ�)��������___________________________________________��
(3)��Һ1���ɳ��������ӷ�Ӧ����ʽΪ_________________________________________��
(4)����pH=8��Ŀ����������һ��___________________������ʹVO2+ת��ΪVO3-����ʱ��Һ��VO2+��VO3-�����ʵ���֮��Ϊa:b��VO2++H2O![]() VO3-+2H+��ƽ�ⳣ��K=____________________��
VO3-+2H+��ƽ�ⳣ��K=____________________��
(5)��Һ2���Ȼ������NH4VO3�����ӷ���ʽΪ__________________________���÷�Ӧ�ܷ�������Ϊ__________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧһѡ��3:���ʽṹ������]
���������ڹ��ý�������������ҪӦ�ã�þ������ͭ�Ǽ�����Ҫ�Ľ���Ԫ�أ���ش���������:
(1)��Ԫ�صĺ˵����Ϊ28����ԭ�ӻ�̬�����Ų�ʽΪ ________ ���ṹ���� ___ �ֲ�ͬ��״�ĵ����ơ�
(2)MgO���۵����CuO��ԭ����__________________________
(3)MgԪ�صĵ�һ�����ܷ����ظ���ͬ���ں�һ��Ԫ�أ�ԭ����_____________________
(4)Ni��CO���γ������Ni(CO)4���÷����ЦҼ���м�������Ϊ _____________________
(5)�����[Cu(CH3C��N)4]BF4��̼ԭ���ӻ��������Ϊ______ ��BF4-�Ŀռ乹��Ϊ_________________ ��
(6)ͭ����Ԫ�ؿ��γ���ͼ��ʾ�ľ����ṹ������Cu���ȵط�ɢ���������ڲ���a��b�������������Ϊ(0,0,0)��(1/2��1/2��1/2)����d���������Ϊ ____________,��֪��Ʒ����ܶ�Ϊ��g/cm3,NA�ǰ����ӵ�����ֵ��������Ϊ _______________ cm(�г�����ʽ����)��
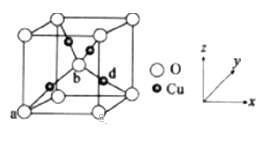
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�����״��ij��÷����ǣ�CO(g)+2H2(g)=CH3OH(g) ��H1=-90.8 kJ/mol��
��֪��2H2(g)+O2(g)=2H2O(1) ��H2=-571.6 kJ/mol
H2(g)+![]() O2(g)=H2O(g) ��H3=-241.8 kJ/mol
O2(g)=H2O(g) ��H3=-241.8 kJ/mol
�����й�˵����ȷ����
A. H2��ȼ����Ϊ241. 8 kJ/mol
B. CH3OH(g)+O2(g)=CO(g)+2H2O(g) ��H=-392. 8 kJ/mol
C. ��![]() ���ȱ�ʾ���Ӹ���Ҳ�ܱ�ʾ���ʵ���
���ȱ�ʾ���Ӹ���Ҳ�ܱ�ʾ���ʵ���
D. δע���¶Ⱥ�ѹǿʱ����H��ʾ��״���µ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ����������ʯī������1 L 1 molL��1ʳ��ˮ�У�����˵����ȷ���ǣ������� 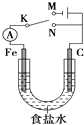
A.�����K��N���ӣ������������ḯʴ
B.�����K��N���ӣ�������Ӧʽ��4OH����4e��=2H2O+O2��
C.�����K��M���ӣ���ʯī������ͭ������ʵ�������϶�ͭ
D.�����K��M���ӣ�������������28 L����״������ʱ��������1 mol NaOH
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com