
 Si3N4 +12HCl
Si3N4 +12HCl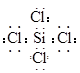 (1分)
(1分) 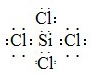 ,故答案为:原子;H、Cl;
,故答案为:原子;H、Cl;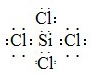 ;
;

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| 选项 | 溶液 | 操作及现象 |
| A | CaCl2溶液 | 通入CO2,溶液不变浑浊;再通入氨气,溶液变浑浊 |
| B | Na2SiO3溶液 | 通入CO2,溶液变浑浊;继续通CO2至过量,浑浊消失 |
| C | Ca(ClO)2溶液 | 通入CO2,溶液变浑浊;再加入品红溶液,红色不褪去 |
| D | BaCl2溶液 | 先通入NO2,再通入SO2至过量,先生成沉淀后沉淀消失 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.普通玻璃的主要成分可以表示为Na2O·CaO·6SiO2,说明玻璃为纯净物 |
| B.陶瓷、玻璃、水泥都属于硅酸盐产品 |
| C.制玻璃、水泥时都用到了石灰石和黏土 |
D.制玻璃的过程中发生了反应:Na2CO3+SiO2 Na2SiO3+CO2↑,说明酸性:H2SiO3>H2CO3 Na2SiO3+CO2↑,说明酸性:H2SiO3>H2CO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.其氧化物都能与NaOH溶液反应 |
| B.其单质在加热时都能跟O2反应 |
| C.其氧化物都能溶于水生成相应的酸 |
| D.碳和硅两种元素共有两种单质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 CO(g)+H2(g) △H=+131.3kJ/mol,达到平衡后,体积不变时,能提高H2O的平衡转化率的措施是 。
CO(g)+H2(g) △H=+131.3kJ/mol,达到平衡后,体积不变时,能提高H2O的平衡转化率的措施是 。| A.升高温度 | B.增加碳的用量 |
| C.加入催化剂 | D.用CO吸收剂除去CO |
 CO2(g)+H2(g)得到如下数据:
CO2(g)+H2(g)得到如下数据:| 温度/℃ | 起始浓度mol/L | 平衡浓度mol/L | |
| CO(g) | H2O(g) | H2(g) | |
| 900 | 2.0 | 0.8 | 0.4 |
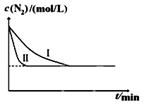
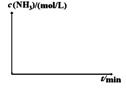
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.硅是制造太阳能电池的常用材料 |
| B.二氧化硅是制造光导纤维的材料 |
| C.水玻璃可用作木材防火剂 |
| D.硅是生产普通玻璃的原料 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.单质硅是良好的半导体材料 |
| B.硅和碳是都是第ⅣA族的元素 |
| C.二氧化硅用来制造通讯材料(光导纤维) |
| D.二氧化硅溶于水生成硅酸,它是挥发性酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com