
 ��1����֪��Fe��s��+$\frac{1}{2}$O2��g��=FeO��s������H=-272.0KJ•mol-1
��1����֪��Fe��s��+$\frac{1}{2}$O2��g��=FeO��s������H=-272.0KJ•mol-1���� ��1�����ݸ�˹������дĿ���Ȼ�ѧ����ʽ��
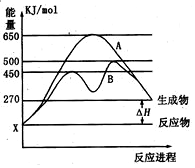
��2������ͼ��֪����Ӧ�����������������������������÷�ӦΪ���ȷ�Ӧ�������¶�ƽ��������Ӧ�����ƶ����ݴ˽��
����ͼ��֪����Ӧ����B��A��ȣ��ı䷴Ӧ���̣�Ӧ��ʹ�ô�����
��3����ѧƽ�ⳣ������ָ��һ���¶��£����淴Ӧ�ﵽƽ��ʱ��������Ũ�ȵĻ�ѧ���������ݵij˻����Ը���Ӧ��Ũ�ȵĻ�ѧ���������ݵij˻����õı�ֵ���ݴ���д��
��4��ȡ0.1mol•L-1HA��Һ��0.1mol•L-1NaOH��Һ�������ϣ���Ϻ���Һ����ı仯���Բ��ƣ�����û��Һ��pH=8����˵��HA�����ᣬ�����������ӵ��δٽ�ˮ���룬
�ٸ�������Һ��pH����ˮ�������c��OH-��������c��NaOH����ˮ�����ӻ���������ˮ��������Ũ�ȣ���Һ��������Ũ�ȵ���ˮ�������c��OH-�����ݴ˽��
�ڸ�������֪��HA�����Ա�̼��ǿ��NH4A��ҺΪ���ԣ�˵��笠����Ӻ��������ˮ��̶���ͬ���ɴ˵�֪笠�����ˮ��̶�С��̼������ӣ����ԣ�NH4��2CO3����Һ�ʼ��ԣ�
��� �⣺��1����Fe��s��+$\frac{1}{2}$O2��g���TFeO��s����H1=-272.0kJ•mol-1
��2Al��s��+$\frac{3}{2}$O2��g���TAl2O3��s����H2=-1675.7kJ•mol-1
������ʽ��-�١�3�ã�2Al��s��+3FeO��s���TAl2O3��s��+3Fe��s����H=-1675.7kJ•mol-1-��3��-272.0kJ•mol-1��=-859.7 kJ•mol-1��
�ʴ�Ϊ��2Al��s��+3FeO��s���TAl2O3��s��+3Fe��s����H=-859.7 kJ•mol-1��
��2������ͼ��֪����Ӧ�����������������������������÷�ӦΪ���ȷ�Ӧ�������¶�ƽ��������Ӧ�����ƶ�����Ӧ���ת��������
�ʴ�Ϊ����������
����ͼ��֪����Ӧ����B��A��ȣ��ı䷴Ӧ���̣����ﵽ��ͬ��ƽ��״̬���ı������Ӧ��ʹ�ô��������ͷ�Ӧ�Ļ�ܣ�
�ʴ�Ϊ��D��
��3��Na2SO4��S��+4H2��g���TNa2S��s��+4H2O��g����ƽ�ⳣ������ʽk=$\frac{{c}^{4}��{H}_{2}O��}{{c}^{4}��{H}_{2}��}$��
�ʴ�Ϊ��$\frac{{c}^{4}��{H}_{2}O��}{{c}^{4}��{H}_{2}��}$��
��4��������Һ��c��OH-��=$\frac{1{0}^{-14}}{1{0}^{-8}}$=10-6 mol/L��0.1mol•L-1NaOH��Һ��c��H+��������ˮ�����������������Ũ�ȣ���c��H+��=cˮ������OH-��=$\frac{1{0}^{-14}}{0.1}$=10-13 mol/L�����Ի��Һ����ˮ�������OH-Ũ����0.1mol•L-1NaOH��Һ����ˮ�������OH-Ũ��֮��=10-6 mol/L��10-13 mol/L=107��1��
�ʴ�Ϊ��107��1��
�ڽ�HA��Һ�ӵ�Na2CO3��Һ��������ų���˵��HA�����Ա�̼���ǿ��NH4A��ҺΪ���ԣ�˵����ͬ�����£���ˮ��HA�ĵ���̶���ͬ�����ԣ�NH4��2CO3��笠����ӵ�ˮ��̶�С��̼������ӵ�ˮ��̶ȣ�������Һ��pH��7��
�ʴ�Ϊ������
���� �����ۺ��Խϴ�ѧ��Ӧ�����仯ͼ������жϣ���Ӧ��ܺ��ʱ������Ӧ�ã��������Һ�йؼ��㡢����ˮ��ȣ��Ƕ�ѧ���ۺ������Ŀ��飬���ջ����ǹؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
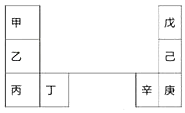 �ס�����Ԫ�������ڱ��е����λ������������ԭ���������3�����һ�ֵ�������Ȼ��Ӳ���������ʣ������ж���ȷ���ǣ�������
�ס�����Ԫ�������ڱ��е����λ������������ԭ���������3�����һ�ֵ�������Ȼ��Ӳ���������ʣ������ж���ȷ���ǣ�������| A�� | �����ԣ��ף��ң��� | |
| B�� | ԭ�Ӱ뾶������������ | |
| C�� | ������ԭ�Ӻ�����������11 | |
| D�� | �ҵĵ����ڿ�����ȼ������ֻ�����Ӽ��Ļ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
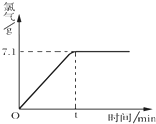 �Ȼ�����һ����Ҫ�Ļ���ԭ�ϣ�����Ȼ�����Һ���Ƶ��������������Ƶ����ʣ������Ļ�ѧ��Ӧ���£�2NaCl+2H2O$\frac{\underline{\;���\;}}{\;}$Cl2��+H2��+2NaOH����ȡһ��������������������Ϊ10%���Ȼ�����Һ���е�⣬���Ȼ�����ȫ��Ӧʱ��ֹͣͨ�磮����������������ʱ��Ĺ�ϵ��ͼ��ʾ������㣺
�Ȼ�����һ����Ҫ�Ļ���ԭ�ϣ�����Ȼ�����Һ���Ƶ��������������Ƶ����ʣ������Ļ�ѧ��Ӧ���£�2NaCl+2H2O$\frac{\underline{\;���\;}}{\;}$Cl2��+H2��+2NaOH����ȡһ��������������������Ϊ10%���Ȼ�����Һ���е�⣬���Ȼ�����ȫ��Ӧʱ��ֹͣͨ�磮����������������ʱ��Ĺ�ϵ��ͼ��ʾ������㣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���� | NaHCO3 | Na2CO3 | NaCN |
| pH | 9.7 | 11.6 | 11.1 |
| A�� | �����ӵ����ʵ���Ũ��֮�ͣ�Na2CO3��NaCN��NaHCO3 | |
| B�� | ��ͬ�����µ����ԣ�H2CO3��HCN | |
| C�� | ������Һ�о����ڵ���ƽ���ˮ��ƽ�� | |
| D�� | ��0.2 mol•L-1NaHCO3��Һ�м�������0.1 ol•L-1 NaOH��Һ��c��CO32-����c��HCO3-����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
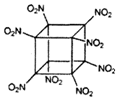 ��ѧ�����Ƴ��İ����������飨�ṹ��ͼ��ʾ��̼ԭ��δ��������һ��������ըҩ����ը�ֽ�õ������ȶ������壮����˵��������ǣ�������
��ѧ�����Ƴ��İ����������飨�ṹ��ͼ��ʾ��̼ԭ��δ��������һ��������ըҩ����ը�ֽ�õ������ȶ������壮����˵��������ǣ�������| A�� | ������C��N���γɼ��Թ��ۼ� | B�� | 1mol�÷����к�8mol-NO2 | ||
| C�� | �����ʼ������������л�ԭ�� | D�� | �����ʱ�ը������NO2��CO2��H2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com