
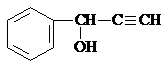 、
、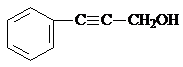 .
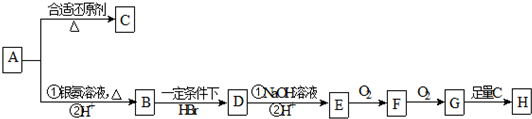
.分析 烃的含氧衍生物A的密度是H2的28倍,则Mr(A)=28×2=56,分子中碳和氢元素总相对原子质量为56×71.4%=40,故含有1个O原子,分子中最大C原子数目为$\frac{40}{12}$=3…4,由于2个碳原子最多需要6个氢原子饱和,故分子中含有3碳原子、4个原子,则A的分子式为C3H4O,A能与银氨溶液反应,说明含有-CHO,不饱和度为2,分子中还含有1个碳碳双键,故A的结构简式为CH2=CH-CHO,A发生还原反应生成C,而C能使溴的四氯化碳溶液褪色,则醛基被还原为羟基,故C为CH2=CHCH2OH,A发生氧化反应、酸化生成B为CH2=CH-COOH,B与HBr发生加成反应生成D,则D为卤代烃,D发生水解反应生成E为醇,E可以连续发生氧化反应,故D为BrCH2CH2COOH,则E为HOCH2CH2COOH,F为OHCCH2COOH,G为HOOCCH2COOH,G与足量的C发生酯化反应生成H,而H的化学式为C9H12O4,则H为CH2=CHCH2OOCCH2COOCH2CH=CH2,据此解答.
解答 解:烃的含氧衍生物A的密度是H2的28倍,则Mr(A)=28×2=56,分子中碳和氢元素总相对原子质量为56×71.4%=40,故含有1个O原子,分子中最大C原子数目为$\frac{40}{12}$=3…4,由于2个碳原子最多需要6个氢原子饱和,故分子中含有3碳原子、4个原子,则A的分子式为C3H4O,A能与银氨溶液反应,说明含有-CHO,不饱和度为2,分子中还含有1个碳碳双键,故A的结构简式为CH2=CH-CHO,A发生还原反应生成C,而C能使溴的四氯化碳溶液褪色,则醛基被还原为羟基,故C为CH2=CHCH2OH,A发生氧化反应、酸化生成B为CH2=CH-COOH,B与HBr发生加成反应生成D,则D为卤代烃,D发生水解反应生成E为醇,E可以连续发生氧化反应,故D为BrCH2CH2COOH,则E为HOCH2CH2COOH,F为OHCCH2COOH,G为HOOCCH2COOH,G与足量的C发生酯化反应生成H,而H的化学式为C9H12O4,则H为CH2=CHCH2OOCCH2COOCH2CH=CH2,
(1)A为CH2=CH-CHO,分子中含氧官能团为醛基,故答案为:醛基;
(2)C的结构简式为CH2=CHCH2OH,B发生加成反应生成D,所以反应类型是加成反应,
故答案为:CH2=CHCH2OH;加成反应;
(3)①该反应为催化氧化反应,反应方程式为2HOCH2-CH2COOH+O2$→_{△}^{催化剂}$2OHCCH2COOH+2H2O,
故答案为:2HOCH2-CH2COOH+O2$→_{△}^{催化剂}$2OHCCH2COOH+2H2O;
②该反应为酯化反应,反应方程式为HOOCCH2COOH+2CH2=CHCH2OH$?_{△}^{浓硫酸}$CH2=CHCH2OOCCH2COOCH2CH=CH2+2H2O,
故答案为:HOOCCH2COOH+2CH2=CHCH2OH$?_{△}^{浓硫酸}$CH2=CHCH2OOCCH2COOCH2CH=CH2+2H2O;
(4)①A的结构简式为CH2=CHCHO,某芳香族化合物M,说明M中含有苯环,与A含有相同类型和数目的官能团,说明A中含有碳碳双键和醛基,且相对分子质量比A大76,一个苯基式量为77,A的式量是55,可知苯中一个H原子被-CH=CHCHO取代,所以A的分子式为C9H8O,故答案为:C9H8O;
②M的同分异构体符合下列条件:
a.苯环上只有一个取代基;
b.能与金属Na反应,但官能团不直接相连,说明含有醇羟基或酚羟基;
c.属于芳香族化合物,不与FeCl3溶液发生显色反应,说明不含酚羟基,则符合条件的同分异构体结构简式为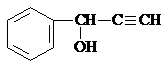
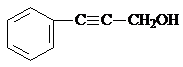
故答案为: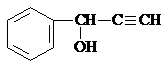
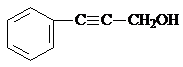
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,正确判断A的结构简式是解本题关键,根据反应条件进行推断,难点是同分异构体种类判断,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 2.5mol•L-1 | B. | 3mol•L-1 | C. | 3.5mol•L-1 | D. | 4mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
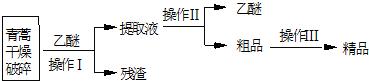
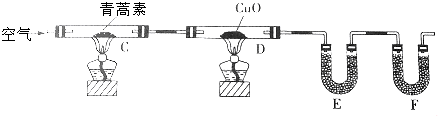
| 装置 | 实验前/g | 实验后/g |
| E | 22.6 | 42.4 |
| F | 80.2 | 146.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
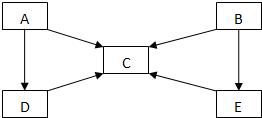 A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如图所示.
A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如图所示. .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 加入10mL 的水进行稀释 | B. | 加水稀释成100mL | ||
| C. | 加入45mL 0.01mol/L的NaOH溶液 | D. | 加入10mL 0.01mol/L的盐酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

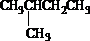

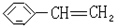 苯乙烯
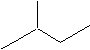
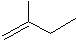
苯乙烯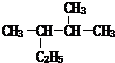 2,3-二甲基戊烷
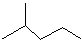
2,3-二甲基戊烷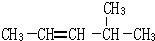 4-甲基-2戊烷
4-甲基-2戊烷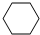 环己烷.
环己烷.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 空气质量日报列入的首要主要污染物有二氧化硫、二氧化氮和可吸入颗粒物等 | |
| B. | 酸雨是指pH小于7的雨水 | |
| C. | 为了减少二氧化硫和二氧化氮的排放,工业废气排放到大气之前必须进行回收处理 | |
| D. | 含磷合成洗涤剂直接排放会导致水体污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com