
| A. | 4.48L | B. | 5.6L | C. | 6.72L | D. | 13.44L |
分析 电解硫酸铜和氯化钠溶液时,阳极上氯离子先放电,然后氢氧根离子放电,阴极上铜离子放电,后氢离子放电,当阴极上析出析出铜的物质的量为0.3mol<0.4mol,根据转移电子守恒计算阳极上生成气体体积.
解答 解:电解硫酸铜和氯化钠溶液时,阳极上氯离子先放电,然后氢氧根离子放电,阴极上铜离子放电,后氢离子放电,当阴极上析出析出铜的物质的量为0.3mol,阴极上转移电子的物质的量=0.3mol×2=0.6mol,
根据原子守恒知,溶液中n(Cl-)=0.2mol,氯离子完全放电时转移电子的物质的量=0.2mol×1=0.2mol,生成氯气0.1mol;
所以阳极上有氧气生成,电极上电子转移为0.4mol,4OH--4e-=2H2O+O2↑,电极反应计算生成氧气0.1mol,所以阳极生成气体物质的量为0.2mol,标准状况下气体的体积为4.48L,
故选:A.
点评 本题以电解原理为载体考查了物质的量的有关计算,明确阳极上析出气体的成分再结合转移电子相等即可解答,题目难度中等.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
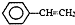 ),聚苯乙烯的化学式为
),聚苯乙烯的化学式为
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | H-H | O═O | O-H |
| 断开1mol化学键所需的能量/kJ | 436 | x | 463 |
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1mol CO (g)和2mol H2(g) | 1mol CH3OH(g) |
| 平衡时c(CH3OH) | c1 | c2 |
| 平衡时能量变化 | 放出54kJ | 吸收a kJ |
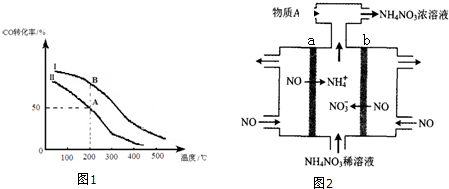
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第5周期第IA族 | B. | 第4周期第IA族 | C. | 第3周期第IA族 | D. | 第3周期第IA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将碳、氢元素符号省略,只表示分子中键的连接情况 | |
| B. | 每个拐点、交点、端点均表示有一个碳原子 | |
| C. | 每一条线段代表一个共价键,每个碳原子有四条线段,用四减去线段数即是氢原子数 | |
| D. | C=C、C≡C键等官能团中的“=”和“≡”也可以省略 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚二氧化碳塑料是通过加聚反应制得的 | |
| B. | 聚二氧化碳塑料与干冰互为同素异形体 | |
| C. | 聚二氧化碳塑料与干冰都属于纯净物 | |
| D. | 聚二氧化碳塑料的使用会产生白色污染 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com