
【题目】下列表示对应化学反应的离子方程式正确的是( )
A.过量石灰水与碳酸氢钙反应:Ca2++2HCO ![]() +2OH﹣═=CaCO3↓+CO
+2OH﹣═=CaCO3↓+CO ![]() +2H2O
+2H2O
B.FeS04酸性溶液暴露在空气中:4Fe2++O2+4H+═Fe3++2H2O
C.向稀HNO3中滴加Na2SO3溶液:SO ![]() +2H+═SO2↑+H2O
+2H+═SO2↑+H2O
D.酸性溶液中KlO3与KI反应生成I2:IO ![]() +I﹣+6H+═I2+3H2O
+I﹣+6H+═I2+3H2O
科目:高中化学 来源: 题型:
【题目】下列离子方程式中,正确的是( )
A.铁与稀硫酸反应 Fe+2H+═Fe3++H2↑
B.氯化铝溶液与氨水反应:Al3++3OH﹣═Al(OH)3↓
C.碳酸钙与稀盐酸反应:CO ![]() +2H+═H2O+CO2↑
+2H+═H2O+CO2↑
D.氢氧化铝与足量盐酸反应 Al(OH)3+3H+═Al3++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势,如图所示: 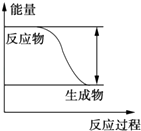
(1)该反应为反应(填“吸热”或“放热”).
(2)若要使该反应的反应速率加快,下列措施可行的是(填字母).
A.改铁片为铁粉
B.改稀硫酸为98%的浓硫酸
C.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为极(填“正”或“负”); 铜电极上发生的电极反应为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列反应的反应方程式:
(1)NaOH溶液吸收氯气的反应:
(2)铁与水蒸气在高温下的反应:
(3)氢氧化铁溶于盐酸:
(4)铝单质溶解在氢氧化钠溶液中:
(5)过氧化钠与二氧化碳反应: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“嫦娥一号”的四大科学目标之一是探测下列14种元素在月球上的含量和分布:K、Th(钍)、U(铀)、O、Si、Mg、Al、Ca、Fe、Ti(钛)、Na、Mn、Cr(铬)、Gd(钆),其中属于短周期元素的有( )
A. 5种B. 7种C. 8种D. 9种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁晶体(FeSO47H2O)在医药上作补血剂.某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质.实验步骤如下: 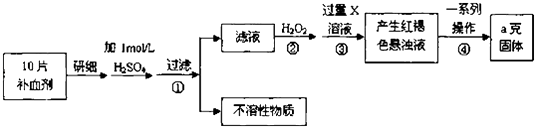
请回答下列问题:
(1)步骤①滤液中滴加KSCN溶液后滤液变为红色,则该溶液中含有(填离子符号),检验滤液中还存在Fe2+的方法为(注明试剂、现象).
(2)步骤②加入过量H2O2的目的是 .
(3)步骤③中反应的离子方程式为 .
(4)步骤④中一系列处理的操作步骤包括:过滤、、灼烧、、称量.
(5)若实验无损耗,则每片补血剂含铁元素的质量为g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于乙酸的下列说法不正确的是( )
A.乙酸是一种重要的有机酸,是具有强烈刺激性气味的液体
B.乙酸分子中含有四个氢原子,所以乙酸是四元酸
C.无水乙酸又称冰醋酸,它是纯净物
D.乙酸易溶于水和乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:常温下,0.01 mol/L MOH溶液的pH为10,MOH(aq)与H2SO4(aq)反应生成1 mol正盐的ΔH=-24.2 kJ·mol-1,强酸与强碱的稀溶液的中和热为ΔH=-57.3 kJ·mol-1。则MOH在水溶液中电离的ΔH为( )
A. -69.4 kJ·mol-1 B. -45.2 kJ·mol-1
C. +69.4 kJ·mol-1 D. +45.2 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式中,书写正确的是( )
A.Fe与稀盐酸反应:2Fe+6H+═2Fe3++3H2↑
B.实验室制备氢氧化铝:Al3++3NH3?H2O═Al(OH)3↓+3NH ![]()
C.氯气与水反应:Cl2+H2O═2H++Cl﹣+ClO﹣
D.铜与稀硝酸反应:Cu+2NO ![]() +4H+═Cu2++2NO2↑+2H2O
+4H+═Cu2++2NO2↑+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com