
【题目】乙烯与水加成制备乙醇的能量变化过程如下图所示。下列说法不正确的是
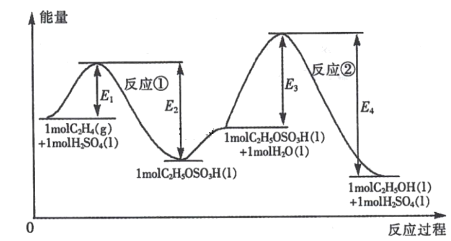
A.H2SO4是该合成过程的催化剂
B.合成过程的速率由反应②决定
C.反应①和反应②均为放热反应
D.C2H4 (g) +H2O(1) =C2H5OH(l )△H =(E1- E4)kJ mol-1
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】化合物A能使溴水褪色,E能与NaHCO3反应,且标准状况下1molE与足量Na反应能产生11.2L气体。A的一系列反应如图(部分反应条件及产物略去):
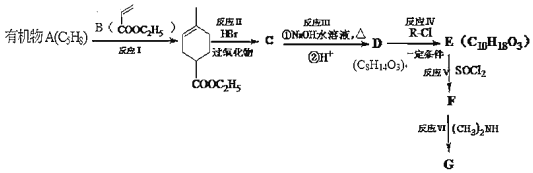
已知:(1)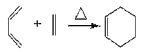
(2)![]()
![]()
![]()
(3)RCOOH![]() RCOCl
RCOCl ![]() RCON(CH3)2
RCON(CH3)2
回答下列问题:
(1)D的结构简式为______
(2)下列说法不正确的是______
A.有机物E中的官能团是羧基和酯基 B.有机物C的分子式为C10H17O2Br
C.反应Ⅲ、Ⅳ、Ⅴ、Ⅵ均属于取代反应 D.1mol有机物E最多可消耗2mol NaOH
(3)写出F→G反应的化学方程式______
(4)写出C5H9NO2满足下列条件的2种链状同分异构体的结构简式。
①红外光谱检测表明分子中含有醛基;②1H-NMR谱显示分子中有3种氢原子。______,______
(5)请设计以有机物A为原料合成(![]() )的合成路线______(用流程图表示,无机试剂任选)。
)的合成路线______(用流程图表示,无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A是一种重要的化工原料,分子中碳与氢元素的质量比为6:1,,是同系物中最简单的物质。X为有浓郁香味、不易溶于水的油状液体。它们之间的转化关系如图:
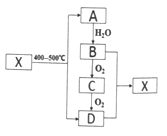
请回答:
(1)有机物D中含有的官能团名称是_________。
(2)A→B的反应类型是_______________。
(3)有机物X在400~500℃下转化为A和D的化学方程式是_____________________。
(4)下列说法正确的是_______________。
A.工业上获得A的的主要方法是催化裂化
B.将绿豆大小的钠投入到B中,钠块浮在液面上,并产生气泡
C.除去C中的D可以先加饱和碳酸钠溶液再蒸馏
D.一定条件下,1molX与足量NaOH溶液反应时,最多消耗1molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芴酮可用作工程塑料的改进剂。某芴酮可通过下列反应得到:
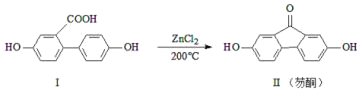
①化合物Ⅱ中含氧官能团为_____和_____(写名称)。
②鉴别化合物Ⅰ和化合物Ⅱ可用的试剂为_____(写化学式)。
③1mol化合物Ⅰ最多可与_____molNaOH完全反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)甲醇(CH3OH)是一种重要的化工原料。已知
CH3OH(1) + O2(g) = CO(g) + 2H2O(g) ; △H = -443.64 kJ·mol-1
2CO (g) + O2(g) = 2CO2(g) ; △H = -566.00 kJ·mol-1
H2O(1) = H2O (g) ; △H = +44.00 kJ·mol-1
①试写出能表示CH3OH(l)燃烧热的热化学方程式:________________________________。试利用热化学方程式计算,完全燃烧16g甲醇生成CO2和H2O(l)时,放出的热量为__________kJ。
②科研人员新近开发出一种由甲醇和氧气以强碱做电解质溶液的新型手机电池。据此回答下列问题:氧气在________极反应;通入甲醇的电极反应式为________________________________。
(2)800℃时A、B、C三种气体在恒容密闭容器中反应时的浓度变化如图所示,分析图像,回答下列问题:
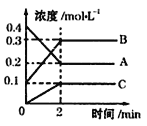
①该反应的方程式为_____________________________________________。
②2min内,用B表示的反应速率为__________________。
③下列能说明该反应达到平衡状态的是_______________。
A.体系压强保持不变 B.容器中气体密度保持不变
C.混合气体平均摩尔质量保持不变 D.每消耗2mol A的同时生成1mol C
E. A、B、C浓度之比为2:2:1 F.混合气体中A的质量分数保持不变
④为加快该反应的反应速率,可采取的措施是_______________。
A.恒容通入He B.分离出B C.选择高效的催化剂 D.适当升高体系温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O反应中,
(1) ______ 元素被氧化, ______ 是氧化剂;
(2) ______ 是氧化产物, ______ 发生氧化反应;
(3)被还原的HNO3与参加反应的HNO3物质的量之比是 ______;
(4)用双线桥标出该反应电子转移的方向和数目:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O_________________;
(5)当有8mol HNO3被还原时,反应转移___________个电子;
(6)写出该反应的离子反应方程式___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一包固体粉末,其中可能含有如下五种物质:CaCO3、K2CO3、Na2SO4、NaCl、CuSO4。现进行如下实验:①溶于水得无色溶液,溶液中无沉淀出现;②向溶液中加入BaCl2溶液生成白色沉淀,再加盐酸时沉淀消失。根据上述实验现象推断:
(1)一定不存在的物质是_____________________;
(2)写出加入盐酸时沉淀消失的离子反应方程式___________________________;
(3)可能存在的物质是___________;
(4)写出下列物质在水溶液中的电离方程式
H2CO3:___________________________;
NH4HCO3 :___________________________;
Ca(OH)2:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,0.1 mol N2(g)与0.3 mol H2(g)在恒容密闭容器中发生反应:N2(g)+3H2(g) ![]() 2NH3(g)ΔH=-akJ·molˉ1(a>0)。下列说法正确的是
2NH3(g)ΔH=-akJ·molˉ1(a>0)。下列说法正确的是
A.容器内气体的压强不再发生变化,说明反应达到平衡状态
B.达到化学平衡状态时,正、逆反应速率都为零
C.相同时间内,断开H—H键的数目和生成N-H键的数目相等
D.平衡时容器内气体的浓度c(N2)∶c(H2)∶c(NH3)=1∶3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象得出的结论正确的是( )
选项 | 实验操作 | 现象 | 结论 |
A | 将电石与水反应产生的气体通入酸性高锰酸钾溶液 | 溶液紫色褪去 | 证明有乙炔生成 |
B | 取CH3COONa溶液于试管中并加入几滴酚酞,再加热 | 溶液红色加深 | CH3COONa溶液显碱性且存在水解平衡 |
C | 向蔗糖溶液中加入稀硫酸,加热几分钟后加入新制Cu(OH)2悬浊液,加热煮沸 | 无红色沉淀生成 | 蔗糖没有发生水解反应生成葡萄糖 |
D | 向Na2S2O3溶液中滴加H2SO4溶液至过量 | 一段时间后溶液变浑浊 | Na2S2O3在该反应中只作氧化剂 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com