
| A. | 纯净物中一定存在化学键 | |
| B. | 阴、阳离子间通过静电引力而形成的化学键叫做离子键 | |
| C. | 只有金属元素和非金属元素化合时才能形成离子键 | |
| D. | 离子化合物中可能含共价键,共价化合物中不含离子键 |
分析 A.稀有气体的单质不含化学键;
B.离子键为静电作用力;
C.金属元素和非金属元素可形成离子键或共价键;
D.含离子键的一定为离子化合物.
解答 解:A.稀有气体的单质不含化学键,则纯净物中不一定都存在化学键,故A错误;
B.离子键为静电作用力,含斥力和吸引力,则阴、阳离子间通过静电作用力而形成的化学键叫做离子键,故B错误;
C.金属元素和非金属元素可形成离子键或共价键,如氯化铝中含共价键,故C错误;
D.含离子键的一定为离子化合物,可能含共价键,如NaOH等,共价化合物中不含离子键,故D正确;
故选D.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,综合性较强,注意特殊物质中的化学键,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4Cl | B. | (NH4)2CO3 | C. | NaCl | D. | K2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
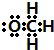 ]-.
]-.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 开发核能、太阳能、氢能等新能源,使用无磷洗涤剂都可直接降低碳排放 | |
| B. | 动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程 | |
| C. | 化石燃料和植物燃料燃烧时放出的能量均来源于太阳能 | |
| D. | 针对节能减排需要大力建设火力发电站 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com