
【题目】下列操作容易造成蔬菜中的维生素损失的是( )
A.洗菜:要先洗后切
B.浸泡:切好的菜要浸泡半天,以除去残留农药
C.切菜:要随切随炒,切忌切好后久置
D.烹饪:烹调蔬菜时适当加点醋,可以减少维生素C的损失
科目:高中化学 来源: 题型:
【题目】苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。
下面是它的一种实验室合成路线:

制备苯乙酸的装置示意图如右(加热和夹持装置等略):
已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。
回答下列问题:
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是_____________________________。
(2)将a中的溶液加热至100 ℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130 ℃继续反应。在装置中仪器c的作用是_______________________。反应结束后加适量冷水,再分离出苯乙酸粗品。加入冷水的目的是___________________。下列仪器中可用于分离苯乙酸粗品的是_______________。
A.分液漏斗 B.漏斗 C.烧杯 D.直形冷凝管 E.玻璃棒
(3)提纯粗苯乙酸的方法是__________________________________________。
(4)将苯乙酸加入到乙醇与水的混合溶剂中充分溶解后,加入Cu(OH)2搅拌30min,过滤。滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于能量转换的认识不正确的是( )
A.电解水生成氢气和氧气时,电能转化为化学能
B.煤燃烧时,化学能主要转化为热能
C.绿色植物进行光合作用时,太阳能转化为化学能
D.白炽灯工作时,化学能主要转化为光能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】120 mL含有0.20 mol碳酸钠的溶液和200 mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是( )
A. 2.0 mol·L-1 B. 1.5 mol·L-1 C. 0.18 mol·L-1 D. 0.24 mol·L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】格氏试剂在有机合成方面用途广泛,可用卤代烃和镁在醚类溶剂中反应制得。设R为烃基,已知:
①RX +Mg![]() R-MgX(格氏试剂);
R-MgX(格氏试剂);
②
阅读以下合成路线图,回答有关问题:
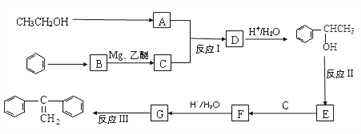
(1)反应I的类型是_____________,反应II的条件是___________________ 。
(2)反应III的化学方程式为____________________________________ 。
(3)E的同分异构体中,含有苯环且能发生银镜反应的有机物共有____种。
(4)有机物 ![]() 是合成药物中的一种原料,实验室可用下列合成路线合成该有机物:
是合成药物中的一种原料,实验室可用下列合成路线合成该有机物:
其中Z的结构简式为________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一定量含有Na2O杂质的Na2O2试样,欲测定Na2O2试样的纯度。可供选用的反应物只有CaCO3固体、6mol·L-1硫酸、6mol·L-1盐酸和蒸馏水。已知:①浓硫酸有吸水性、脱水性和强氧化性,②碱石灰的成分为CaO和NaOH。实验方案为:①制备并提纯CO2。②将纯净的CO2通过试样。③测定生成O2的体积。④根据O2的体积计算Na2O2试样的纯度。实验装置如下:

回答下列问题:
(1)装置A中发生反应的离子方程式是______________________________________。
(2)装置B的作用是_______________________,装置C的作用是_______。
(3)装置E的作用是__________________________________________
(4)装置D中发生反应的化学方程式是______________________________________。
(5)若开始时测得样品的质量为2.0g,反应结束后测得气体体积为224mL(标准状况),则Na2O2试样的纯度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为淡黄色固体,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀。

(1)物质A的化学式为 ________。
(2)H在潮湿空气中变成M的实验现象是______________________________________,化学方程式为___________________________________________。
(3)A和水反应生成B和C的离子方程式为___________________________________,由此反应可知A有作为_________的用途。
(4)步骤①的离子方程式_______________________________________,请写出检验步骤①得到的溶液中主要阳离子(除H+外)所需要的试剂:_____________、____________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有X-、Y2-、Z2-三种常见的无机离子。如下图所示,发生了一系列化学反应。第④步反应生成的白色沉淀中含Y2-.

(1)判断X-、Y2-、Z2-分别为________、________、________(写离子符号)。
(2)写出④、⑤步反应的离子方程式。
④______________________________________________________;
⑤______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列物质中①NaCl晶体 ②液态S03 ③醋酸 ④汞 ⑤BaS04固体 ⑥酒精 ⑦熔化的KN03 属于电解质的是(填序号)_________________________
(2)质量为3.9 g的Na2X中含有Na+的物质的量为0.1mol,则Na2X的摩尔质量为______,
(3)某气体对氧气的相对密度为2,则此气体的相对分子质量为______
(4)3.01×1022个S2-的物质的量为________,质量为________,含有质子的物质的量为______,含有电子的物质的量为________。
(5)某地酸雨经检验,除含氢离子外,还有如下离子:c(Na+)=1.4×10-3 mol·L-1 ,c(Cl-) =3.5×10-3 mol·L-1 ,c(NH) =2.3×10-3 mol·L-1 , c(SO![]() ) =1.5×10-3 mol·L-1。则该溶液中氢离子的浓度为_____________ mol·L-1。
) =1.5×10-3 mol·L-1。则该溶液中氢离子的浓度为_____________ mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com