


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
| ② | |||
| ⑦ | ⑧ |
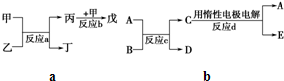
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该反应中旧键断裂所吸收的能量大于新键形成所放出的能量 |
| B.该反应放出热量的多少与反应物的用量有关 |
| C.该反应的化学能可以转化为电能 |
| D.反应物的总能量高于生成物的总能量 |
查看答案和解析>>
科目:高中化学 来源:2010-2011学年湖北省黄冈市英山一中高一(下)月考化学试卷(4月份)(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com