
| A. | 直接用酒精喷灯加热 | B. | KMnO4、铝条 | ||
| C. | 火柴头、浓盐酸 | D. | KMnO4、鞭炮引线 |
分析 为使反应顺利进行,加入的氯酸钾为助燃剂,点燃镁时反应可发生,镁为引燃剂,所以选项中必须提供代替镁的引燃剂、代替氯酸钾的助燃剂,据此进行解答.
解答 解:铝热反应中,为使反应顺利进行,可加入氯酸钾,为助燃剂,点燃镁时反应可发生,镁为引燃剂,
A.根据铝热反应装置可知,无法用酒精喷灯对反应的混合物进行加热,故A错误;
B.缺少引燃剂,铝热反应不会发生,故B错误;
C.火柴头可以做引燃剂,但是缺少助燃剂,无法达到反应所需温度,故C错误;
D.鞭炮引线为引燃剂,高锰酸钾为助燃剂,铝热反应可以发生,故D正确;
故选D.
点评 本题考查了放热反应发生条件,题目难度不大,注意掌握铝热反应原理,明确镁条、氯酸钾在铝热反应中的作用为解答本题的关键,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:解答题

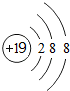 .
.| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为红色 | 氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | _氯气与水反应生成的HClO将石蕊氧化为无色物质 |
| 然后溶液从无色逐渐变为浅黄绿色 | 继续通入的氯气溶于水使溶液呈浅黄绿色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 CO和H2作为重要的燃料和化工原料,有着十分广泛的应用.
CO和H2作为重要的燃料和化工原料,有着十分广泛的应用.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
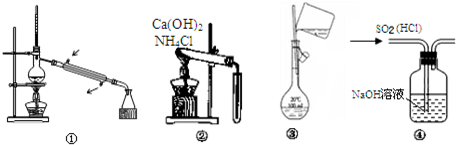
| A. | 图①常用于分离沸点不同且彼此互溶的液态混合物 | |
| B. | 图②可用于实验室制备并收集少量的NH3 | |
| C. | 图③表示的是实验室配制溶液转移过程 | |
| D. | 图④可用于除去SO2中的HCl气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
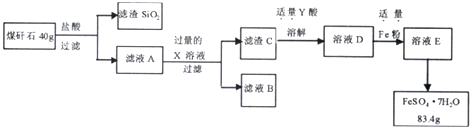
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com