
Mg和SiO2在高温下反应生成MgO和Mg2Si。下列说法正确的是
A.微粒的半径:Si > Mg B.氧元素不存在同素异形体
C.Mg的还原性强于Si D.该反应是置换反应,镁元素被氧化
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2016届河南省南阳市高三上学期期中质量评估化学试卷(解析版) 题型:选择题
(NH4)2SO4在一定条件下发生如下反应:4(NH4)2SO4=N2 +6NH3 +3SO2 +SO3+7H2O,将反应后的混合气体通入Ba(NO3)2溶液,产生的沉淀为
A. BaSO4和BaSO3 B. BaSO4 C.BaSO3 D. BaS
查看答案和解析>>
科目:高中化学 来源:2016届江苏省南通市高三上学期第一次阶段测化学试卷(解析版) 题型:选择题
增塑剂DCHP可由邻苯二甲酸酐与环己醇反应制得。

邻苯二甲酸酐 DCHP
下列说法正确的是
A.邻苯二甲酸酐的二氯代物有3种
B.环己醇分子中所有的原子可能共平面
C.DCHP能发生加成、取代、消去反应
D.1 mol DCHP最多可与含2 mol NaOH的溶液反应
查看答案和解析>>
科目:高中化学 来源:2016届江苏省苏北四市高三上学期期中质量抽测化学试卷(解析版) 题型:填空题
工业上采用硫铁矿焙烧去硫后的烧渣(主要成分为Fe2O3、FeO、SiO2、Al2O3,不考虑其他杂质) 制取七水合硫酸亚铁(FeSO4·7H2O) ,流程如下:

(1)浸取时,溶液中的Fe2+易被空气中的O2氧化,其离子方程式为 。能提高烧渣浸取速率的措施有 (填字母)。
A.将烧渣粉碎 B.降低硫酸的浓度 C.适当升高温度
(2)还原时,试剂X的用量与溶液pH的变化如图所示,则试剂X可能是 (填字母)。

A.Fe粉 B.SO2 C.NaI
还原结束时,溶液中的主要阴离子有 。
(3)滤渣Ⅱ主要成分的化学式为 ;由分离出滤渣Ⅱ后的溶液得到产品,进行的操作是 、 过滤、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源:2016届江苏省苏北四市高三上学期期中质量抽测化学试卷(解析版) 题型:选择题
下列指定反应的离子方程式正确的是
A.氨水吸收少量的CO2气体:NH3·H2O+ CO2 = NH4++HCO3-
B.Na2SO3溶液中SO32-的水解:SO32-+ 2H2O=H2SO3 + 2OH-
C.KClO3溶液与浓盐酸反应: ClO3-+5Cl-+6H+=3Cl2↑+3H2O
D.(NH4)2Fe(SO4)2溶液与过量NaOH反应:Fe2++2OH-=Fe(OH)2↓
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一上学期10月月考化学试卷(解析版) 题型:填空题
实验题:
I.海藻中提取碘的流程如图,已知②中发生反应的化学方程式为:
Cl2+2KI===2KCl+I2。请回答下列问题:
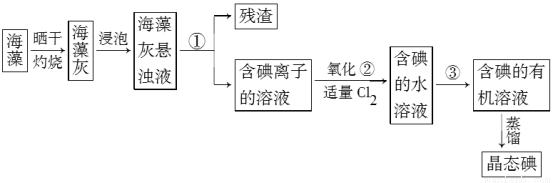
(1)指出提取碘的过程中有关实验操作①、③的名称:________;________。
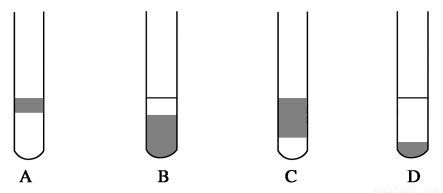
(2)在3mL碘水中,加入1mL四氯化碳,振荡、静置后,观察到试管里的分层现象是________。(注:如图试管中深色区为紫红色溶液)
(3)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏,指出如图实验装置中的错误之处。(加热装置烧杯下已垫石棉网)
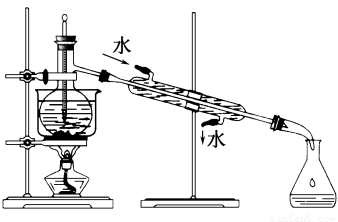
①________________________________________________;
②________________________________________________。
II.某化学兴趣小组在课外活动中,对某溶液进行了多次检测,其中三次检测结果如下表所示,请回答:
检测次数 | 溶液中检测出的物质 |
第一次 | KCl、K2SO4、Na2CO3、NaCl |
第二次 | KCl、BaCl2、Na2SO4、K2CO3 |
第三次 | Na2SO4、KCl、K2CO3、NaCl |
(1)三次检测结果中第________次检测结果肯定不正确。
(2)在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子:
第一步:向溶液中滴加过量的①________溶液(填化学式),其目的是检验CO32-并将其除去;
第二步:加入②________溶液(填化学式),其目的是③_________________________
________________________________________________________________________;
第三步:过滤,再向滤液中加入④________溶液(填化学式),其目的是⑤________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一上学期10月月考化学试卷(解析版) 题型:选择题
某实验小组只领取下列仪器和用品:铁架台、铁夹、铁圈、三角架、石棉网、烧杯、漏斗、分液漏斗、酒精灯、玻璃棒、量筒、蒸发皿、锥形瓶、牛角管、火柴、滤纸。不能进行的实验操作是
A.蒸发 B.萃取 C.过滤 D.蒸馏
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省杭州地区七校高一上学期期中联考化学试卷(解析版) 题型:实验题
海水中有丰富的资源,多种多样的海洋动物和植物,海底有丰富的矿藏、石油、天然气等,此外,海水中还含有大量的电解质,它们电离产生Cl-、Br -、I-、SO42-、Na+、Mg2+、Ca2+等,都是重要资源.开发和利用海水资源是当前科学研究的一项重要任务,如图是某化工厂对海水资源综合利用的示意图:
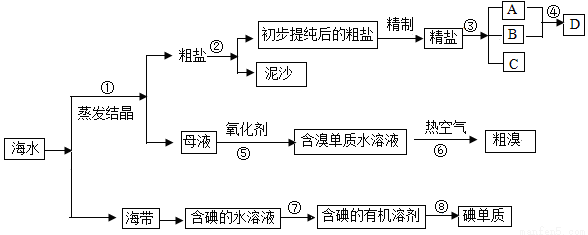
请根据以上信息回答下列问题:
(1)写出步骤②、⑧分离提纯的方法:
② ⑧ 。
(2)步骤⑦分离提纯过程中需要选用的玻璃仪器除烧杯外,还需要的仪器是 。
(3)D具有杀菌消毒的作用,请写出反应④的化学方程式 。
(4)初步提纯后的粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:
①盐酸 ②氯化钡溶液 ③氢氧化钠溶液 ④碳酸钠溶液,
下列试剂添加顺序合理的是 。
A.②③④① B.③④②① C.④③②① D.③②④①
(5)若用来提取Br2,反应⑤所用的氧化剂的来源较合理的是 。
A.从外地购买 B.在当地新建生产厂 C.从本厂生产烧碱处循环
(6)流程⑥将溴单质从水溶液中分离出来是基于溴单质具有 性,该方法对比有机溶剂萃取法的优点是 。
查看答案和解析>>
科目:高中化学 来源:2016届广东省、潮州金中高三上学期期中联考理综化学试卷(解析版) 题型:实验题
焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5。
已知:① 装置Ⅱ中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2===Na2S2O5。
② Na2S2O5晶体在空气中被氧化生成Na2SO4。
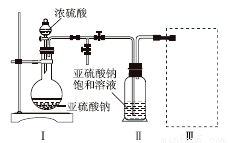
(1) 装置Ⅰ中产生气体的化学方程式为______________________________。
(2) 要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是 。
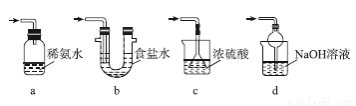
(3) 装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为________(填序号)。
(4) 检测Na2S2O5晶体在空气中已被氧化的实验方案是 ___________________。

(5)为了研究干燥的Cl2与干燥SO2反应及进行程度。用如图所示装置收集满干燥的Cl2,再通入干燥SO2,集气瓶中立即产生无色液体SO2Cl2,充分反应后,将液体和剩余气体分离。继续用NaOH溶液吸收分离出的气体,用足量稀盐酸酸化后,再滴加BaCl2溶液,产生白色沉淀,该白色沉淀是 ,由此可知反应后剩余气必然存在 气体,综合实验信息,请写出干燥的SO2与Cl2反应的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com