
| A. | 由2Cu+O2$\frac{\underline{\;△\;}}{\;}$2CuO可推出同族的硫也有Cu+S$\frac{\underline{\;△\;}}{\;}$CuS | |
| B. | Fe3O4可表示为FeO•Fe2O3,则Pb3O4可表示为PbO•Pb2O3 | |
| C. | Na能与水反应生成H2,K、Ca也能与水反应生成H2 | |
| D. | CO2与Na2O2反应只生成Na2CO3和O2,故SO2与Na2O2反应只生成Na2SO3和O2 |
分析 A.硫与铜反应生成硫化亚铜;
B.Pb的化合价为+2价、+4价,不存在+3价;
C.钾、钠和钙金属的活泼性较强,都能够与水反应;
D.SO2与Na2O2发生氧化还原反应生成Na2SO4.
解答 解:A.S的氧化性较弱,与Cu反应生成Cu2S,正确的方程式为:2Cu+S$\frac{\underline{\;△\;}}{\;}$Cu2S,故A错误;
B.Pb的化合价为+2价、+4价,不存在+3价,Pb3O4可表示为:2PbO•PbO2,故B错误;
C.Na、K、Ca的化学性质比较活泼,都能够与水反应生成氢气,故C正确;
D.SO2与Na2O2发生氧化还原反应生成Na2SO4,没有氧气生成,故D错误;
故选C.
点评 本题考查常见元素及其化合物性质,侧重考查类比规律,题目难度中等,明确常见物质的性质是解答该题的关键,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:解答题
 的名称是2-甲基-2-丁烯
的名称是2-甲基-2-丁烯 的分子式是C10H18O
的分子式是C10H18O查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同质量、不同密度的N2O和CO2 | |
| B. | 相同体积、相同密度的CO和C2H4 | |
| C. | 相同温度、相同压强、相同体积的O2和O3 | |
| D. | 相同压强、相同温度、相同质量的O2和SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 装置Ⅰ:可以用来验证碳的非金属性比硅强 | |
| B. | 装置Ⅱ:橡皮管的作用是使水顺利流下 | |
| C. | 装置Ⅲ:不能检查该装置的气密性 | |
| D. | 装置Ⅳ:先从①口进气收集满二氧化碳,再从②口进气,可收集NO气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 或
或 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na能与冷水反应,而Mg不能 | |
| B. | Na最外层有一个电子,Mg最外层有2个电子 | |
| C. | 碱性NaOH<Mg(OH)2 | |
| D. | Na能从MgCl2 的溶液中把Mg置换出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯的分子式是C6H6,不能使酸性高锰酸钾溶液褪色,属于饱和烃 | |
| B. | 从苯的凯库勒式看,分子中含有双键,所以属于烯烃 | |
| C. | 在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应 | |
| D. | 苯分子为平面正六边形结构,六个碳原子处于同一平面内 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. |  | ||
| C. |  | D. | 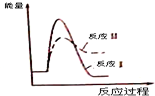 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com