(2010?和平区一模)Ⅰ.某化学兴趣小组探究饱和氯水与石灰石的反应,并制取较浓的HClO溶液和对所得溶液中的部分阴离子进行检验.
|
实验操作 |
实验现象 |
| 步骤1 |
在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,过滤,将滤液分为若干份. |
有少量气泡产生,溶液的黄绿色褪去. |
| 步骤2 |
将第一份滤液与稀盐酸混合. |
产生大量气泡. |
| 步骤3 |
将第二份滤液加热. |
溶液变浑浊,且有大量无色气体产生. |
(1)用平衡移动的观点解释石灰石溶解氯水的原因
将石灰石放在水中有CaCO3(S)=Ca2+(aq)+CO32-(aq)平衡存在,氯水中存在Cl2+H2O?H++Cl-+HClO平衡,加入到氯水中又有2H++CO32-=H2O+CO2↑发生,H+-的浓度减少,平衡正向移动,石灰石溶解了氯水
将石灰石放在水中有CaCO3(S)=Ca2+(aq)+CO32-(aq)平衡存在,氯水中存在Cl2+H2O?H++Cl-+HClO平衡,加入到氯水中又有2H++CO32-=H2O+CO2↑发生,H+-的浓度减少,平衡正向移动,石灰石溶解了氯水
.
(2)步骤2、步骤3的实验目的都是
检验HCO3-离子
检验HCO3-离子
,为达到该实验目的,还可以采取的方法是
另取一份滤液,加入NaOH溶液,观察有无沉淀产生
另取一份滤液,加入NaOH溶液,观察有无沉淀产生
.
(3)请你设计-个简单的实验方案,证明步骤1所得滤液中的HClO浓度比饱和氯水中HClO浓度大:
同时将滤液和饱和氯水滴在有色布条上,比较有色布条褪色的快慢
同时将滤液和饱和氯水滴在有色布条上,比较有色布条褪色的快慢
.
Ⅱ.摩尔盐[(NH
4)
2SO
4?FeSO
4?6H
2O]在空气中比一般亚铁盐稳定,是化学分析中常用的还原剂.某研究性学习小组按以下步骤制取摩尔盐:
①用30%的NaOH溶液和废铁屑混合、煮沸、冷却、分离;
②用①处理过的铁屑和稀H
2SO
4反应制取FeSO
4;
③将②制得的FeSO
4溶液与[(NH
4)
2SO
4溶液混合,结晶得到摩尔盐.
试回答下列问题:
(1)如何从溶液中分解出摩尔盐?
(2)如何设计一个简单的实验证明得到的产品中有Fe
2+?
(3)为了确定产品中亚铁离子的含量,某研究小组用KMnO
4酸性溶液进行滴定,请写出该反应的离子方程式:
MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
.
(4)现有等浓度的①(NH
4)
2CO
3 ②(NH
4)
2SO
4 ③(NH
4)
2Fe(SO
4)
2溶液,其中c(NH
4+)由大到小的顺序是:
③②①
③②①
(填序号).



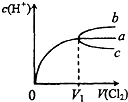 (2010?和平区一模)一定温度下,将Cl2缓慢通入水中.当通入的Cl2体积为V1时达到饱和,溶液中c(H+)变化如图中曲线a.已知Cl2的溶解度随温度升高而迅速降低,下列叙述中正确的是( )
(2010?和平区一模)一定温度下,将Cl2缓慢通入水中.当通入的Cl2体积为V1时达到饱和,溶液中c(H+)变化如图中曲线a.已知Cl2的溶解度随温度升高而迅速降低,下列叙述中正确的是( )