
【题目】NOx会引起光化学烟雾等环境问题,在催化剂存在条件下,以NH3或尿素将尾气中NOx
还原为N2的技术,即NH3或尿素-SCR技术,是去除NOx最为有效且应用最广的技术之一,其中最重要的催化剂体系是钒基催化剂。
(1)NH3去除尾气中的NOx,当v(NO):v(NO2)=l:1时称为“快速SCR 反应”,该反应化学方程式为___________。
(2)不同钒含量的催化剂(V2O5/TiO2)添加WO3对NO去除率的影响如下图,从图中可以得出其它条件相同时添加WO3,对NO去除率的影响是_____(填“增大”、“减小”或“无影响”)。根据图中所示,随着温度升高NO去除率的变化趋势为_____,该变化趋势的一种可能原因是___________。

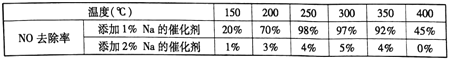
(3)在制备钒基催化剂时,添加的各种成型助剂中碱金属或碱土金属(如Na、K、Ca)能够使催化剂中毒(催化性能下降), K、Ca的毒化作用与Na相似。下列适合做成型助剂有_____。
A.Li B.Mg C.酸性铝溶胶 D.酸性硅溶胶
请设计实验研究添加金属K对催化剂活性的影响(只需写出实验思路,不需要具体实验
操作)_____________。
(4)在NOx催化去除过程中,NH3储罐存在危险性,更多应用为尿素-SCR技术。在该技术过程中,发生如下两个反应:
① CO(NH2)2=NH3+HNCO
② HNCO(g)+H20(g)====NH3(g)+CO2(g)
在此过程中一分子尿素可以生成两分子NH3,因此尿素被视为是NH3的有效储存源。反应②的平衡常数表达式为_______。目前商用的尿素溶液浓度为32.5%(密度为1.05g/mL),常称为“Ad Blue ”。1L该商用尿素溶液发生“快速SCR反应”, 理论上最多可消除NO和NO2在标准状况下的体积为______L。
【答案】 2NH3+NO+NO2= 2N2+3H2O 增大 减小 低温阶段,温度升高反应速率加快导致NO去除率增大;高温阶段,温度升高平衡逆向移动导致NO去除率下降;②低温阶段,温度升高反应速率加快导致NO去除率增大;高温阶段,发生NH3的非选择性氧化NOx反应。③低温阶段,温度升高反应速率加快导致NO去除率增大;高温阶段,催化剂活性下降。(其它合理答案均可) C、D 分别向催化剂中添加1%K、2%K,并控制与(3)题中相同实验条件下,然后测定不同温度下的NO去除率,绘制成图表。 [c(NH3)c(CO2)]/[c(HNCO)c(H2O)] 254.8
【解析】(1)当V(NO):V(NO2)=1:1时称为“快速SCR反应”,根据氧化还原方程式的原理可以书写配平得出:2NH3+NO+NO2= 2N2+3H2O;
(2)本小题要特别注意对图像的分析,根据控制变量的思想,当钒含量相同时可以发现,添加了WO3后,催化剂在各温度下对NO的去除率影响均为增大; 根据图像,其他因素相同时,低温阶段(350℃以下)温度升高NO去除率增大,高温阶段(350℃以上)随着温度升高NO去除率减小;可能的原因有:①低温阶段,温度升高反应速率加快导致NO去除率增大;高温阶段,温度升高平衡逆向移动导致NO去除率下降;②低温阶段,温度升高反应速率加快导致NO去除率增大;高温阶段,发生NH3的非选择性氧化NOx反应。③低温阶段,温度升高反应速率加快导致NO去除率增大;高温阶段,催化剂活性下降;
(3)在制备钒基催化剂时,添加的各种成型助剂中的碱金属或碱土金属(如Na、K、Ca)能够使催化剂中毒(催化性能下降),K、Ca的毒化作用与Na相似。A选项Li为碱金属,B选项Mg为碱土金属,故C、D中酸性铝溶胶和酸性硅溶胶更适合作为成型助剂; 根据表格中的实验情况,可以类似延伸,把握住控制变量的思想便可以设计出实验思路,另外要求绘制成图表,更加直观形象的展示出实验结果:分别向催化剂中添加1%K、2%K,并控制与(3)题中相同实验条件下,然后测定不同温度下的NO去除率,绘制成图表;
(4)根据平衡常数的定义可知:K=[c(NH3)c(CO2)]/[c(HNCO)c(H2O)]
理论上一分子尿素可以生成两分子NH3,所以此处不考虑反应②的可逆性,按照完全反应来进行理论计算,同时发生的是“快速SCR反应”,2NH3+NO+NO2= 2N2+3H2O,1mol CO(NH2)2~2mol NH3~1molNO+1mol NO2,V(NO+NO2)=![]() ×22.4L=254.8L。
×22.4L=254.8L。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等。下列判断不正确的是( )
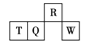
A. 最简单气态氢化物的热稳定性:R>Q
B. 最高价氧化物对应水化物的酸性:Q<W
C. 原子半径:T>Q>R
D. 含T的盐中,T元素只能存在于阳离子中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g)(已知:2SO2+O2![]() 2SO3),反应过程中的能量关系可用右图简单表示(图中的ΔH 表示生成1 mol产物的数据)。 下列说法正确的是( )
2SO3),反应过程中的能量关系可用右图简单表示(图中的ΔH 表示生成1 mol产物的数据)。 下列说法正确的是( )
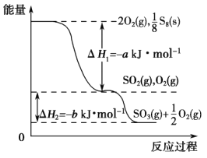
A.S8的燃烧热 ΔH=-a kJ·mol-1
B.1 mol SO2和过量 O2反应可释放出 b kJ 的热量
C.已知1个S8分子中有8个S-S,S=O的键能为d kJ·mol-1,O=O的键能为e kJ·mol-1,则S8分子中S-S的键能为(2d-a-e) kJ·mol-1
D.若使用V2O5作催化剂,当SO2(g)转化生成1mol SO3(g)时,释放的热量小于b kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池总反应的离子方程式是Fe+2Fe3+=3Fe2+ , 该原电池的组成正确的是( )
Zn | A | B | C | D |
正极 | Fe | C(石墨) | Ag | Zn |
负极 | Cu | Fe | Fe | Fe |
电解质溶液 | FeCl3 | Fe2 (SO4)3 | H2SO4 | FeCl3 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L。请回答:
(1)NO的体积为_____L,NO2的体积为______L。
(2)参加反应的硝酸的物质的量是_______mol。
(3)待产生的气体全部释放后,向溶液加入VmL a mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为___________mol/L。(结果不需化简)
(4)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3,至少需要30%的双氧水________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】连二亚硫酸钠(Na2S2O4)俗称保险粉,是一种强还原剂,工业上可通过吸收大气污染物(含有SO2、NO等制取),同时还可得到NH4NO3产品,工艺流程图如下(Ce为铈元素):

请回答下列问题:
(1)装置I中可生成NaHSO3。常温下NaHSO3溶液呈酸性的原因是____________。
(2)装置II中酸性条件下,NO被Ce4+氧化为NO3- 时,氧化产物与还原产物的物质的量之比为______。
(3)装置III中阴极上的电极反应式为__________。若装置IV中NO2- 的浓度为11.5g·L-1要使1dm3该
溶液中的NO2- 完全转化为NH4NO3,至少向装置IV中通入标准状况下的O2__________L。
(4)Na2S2O4在空气中容易被氧化,其反应方程式可能为:
①2Na2S2O4+O2+2H2O=4NaHSO3;
②Na2S2O4+O2+H2O=NaHSO3+ NaHSO4。
请设计实验证明氧化时一定有反应②发生______________。
(5)SO2—空气质子交换膜燃料电池原理示意图如下图:

质子的流动方向为__________(“从A到B”或“从B到A”),负极的电极反应式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】课外学习小组为检验溶液中是否含有常见的四种无机离子,进行了如图所示的实验操作。其中操作过程中产生的气体能使红色石蕊试纸变蓝,由该实验能得到的正确结论是( )
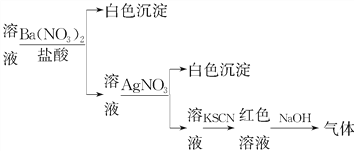
A. 溶液中一定含有SO![]()
B. 溶液中一定含有NH![]()
C. 溶液中一定含有Cl-
D. 溶液中一定含有Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素原子半径与原子序数的关系图.则下列说法正确的是( )

A. 简单离子的半径:X<Z<M
B. 最高价氧化物对应水化物的酸性:R<N
C. Y、R两种元素的气态氢化物稳定性:Y>R
D. 由X与N两种元素组成的化合物不能与任何酸反应,但能与强碱反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了一组实验验证元素周期律。
(Ⅰ)甲同学在a、b、c三只烧杯里分别加入50 mL水,再分别滴加几滴酚酞溶液,依次加入大小相近的锂、钠、钾块,观察现象。
甲同学设计实验的目的是 , 烧杯 (填字母)中的反应最剧烈。
(Ⅱ)乙同学设计实验验证非金属元素的非金属性越强,对应的最高价含氧酸的酸性就越强。他设计了下图装置以验证氮、碳、硅元素的非金属性强弱。

乙同学设计的实验可直接证明三种酸的酸性强弱,已知A是强酸,常温下可与铜反应;B是块状固体;打开分液漏斗的活塞后,C中可观察到有白色沉淀生成。
(1)写出所选用物质的化学式:A: ;B: ; C: 。
(2)写出烧杯中发生反应的离子方程式:
(3)该装置存在着某个缺陷,改进的方法是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com