
| A. | 臭氧被称为绿色氧化剂,无毒无害 | |
| B. | 王水是浓盐酸和浓硝酸按体积比1:3配成的混合物,可以溶解Au、Pt | |
| C. | 氨水能导电,说明氨气是电解质 | |
| D. | 新制备的氯水中存在3种分子、4种离子 |
分析 A.臭氧浓度过大,对人体有害;
B.王水中浓盐酸和浓硝酸的体积比3:1;
C.氨气为非电解质;
D.氯水中含有氯气、水、次氯酸、氢离子、氢氧根离子、氯离子、次氯酸根离子等微粒.
解答 解:A.臭氧被称为绿色氧化剂,但臭氧浓度过大,对人体有害,故A错误;
B.王水中浓盐酸和浓硝酸的体积比3:1,王水为混合物,能溶解Au、Pt,故B错误;
C.氨气本身不能电离,为非电解质,氨气和水反应可生成一水合氨,为电解质,故C错误;
D.氯水中含有氯气、水、次氯酸、氢离子、氢氧根离子、氯离子、次氯酸根离子等微粒,则含有3种分子、4种离子,故D正确;
故选:D.
点评 本题考查较为综合,涉及物质的组成、性质以及应用,侧重于化学与生活、生产的考查,有利于培养学良好的科学素养,难度不大,注意相关基础知识的积累.


科目:高中化学 来源: 题型:多选题
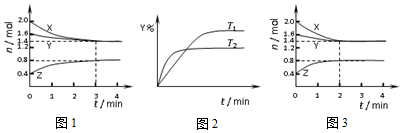
| A. | 容器中发生的反应可表示为:3X(g)+Y(g)?2Z(g) | |
| B. | 保持其他条件不变,升高温度,平衡向X体积分数增大的方向移动 | |
| C. | 反应进行的前3 min内,用X表示的反应速率 v(X)=0.2mol•(L•min)-1 | |
| D. | 若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
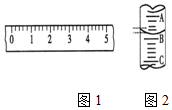 (1)某学生用托盘天平称量一个小烧杯的质量,如小烧杯的质量为32.6g,用“↓”表示在托盘上放砝码,“↑”表示从托盘上取砝码,请用箭头在表中填空,表示称量过程,并在如图1所示的游码尺上画出游码的位置(画“|”表示).
(1)某学生用托盘天平称量一个小烧杯的质量,如小烧杯的质量为32.6g,用“↓”表示在托盘上放砝码,“↑”表示从托盘上取砝码,请用箭头在表中填空,表示称量过程,并在如图1所示的游码尺上画出游码的位置(画“|”表示).| 砝码质量/g | 50 | 20 | 20 | 10 | 5 |
| 取用砝码情况 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
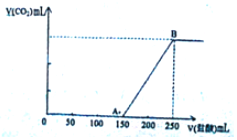 向100mL某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2,充分反应后,向所得溶液中逐滴滴入1mol/L的盐酸溶液,所得气体的体积(标准状态)与所加盐酸的体积关系如图所示
向100mL某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2,充分反应后,向所得溶液中逐滴滴入1mol/L的盐酸溶液,所得气体的体积(标准状态)与所加盐酸的体积关系如图所示查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子中2p能级比2s能级多一个电子的第二周期元素 | |
| B. | 位于元素周期表中第三周期ⅢA族的元素 | |
| C. | 原子最外层电子排布为2s22p6的元素 | |
| D. | 原子最外层电子排布为2s22p5的元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com