
| 物质 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 1.8 | 6.3 | 5.2 |
| 完全沉淀的pH | 3.0 | 8.3 | 6.7 |
分析 Ⅰ.取一定量样品于烧杯中,加足量NaOH溶液,有气体产生,证明一定含有金属铝,过滤得到固体A和无色溶液B,溶液B一定含NaAlO2溶液;
Ⅱ.向B中加入稀硫酸,出现白色沉淀,继续滴加稀硫酸至过量,白色沉淀完全溶解,说明溶液B只有NaAlO2溶液,没有硅酸钠,则推断固体样品不含二氧化硅;
Ⅲ.因为Cu2O+2H+═Cu+Cu2++H2O,向A中加入足量稀硫酸并微热,完全溶解,则必定三价铁生成即Fe2O3或Fe3O4或Fe2O3和Fe3O4,将生成的单质铜氧化成铜离子而全部溶解,所以溶液C必定含过量的氢离子、二价铁、二价铜的混合溶液;
Ⅳ.向C中加入NaClO,将二价铁氧化成三价铁,调节溶液的pH至4~5,产生红褐色沉淀,过滤得到蓝绿色溶液D为二价铜的溶液;
Ⅴ.向D中加入NaOH,调节溶液的pH到7~8,产生蓝色絮状沉淀为氢氧化铜.
综上所述:固体样品中组成为组合1:Al、Fe2O3、Cu2O;组合2:Al、Cu2O、Fe3O4;组合3:Al、Fe2O3、Cu2O、Fe3O4.;一定不含SiO2;依据推断出的物质分析回答.
解答 解:(1)取一定量样品于烧杯中,加足量NaOH溶液,有气体产生,证明一定含有金属铝,方程式为:2Al+2OH-+2H2O═2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑;
(2)由Ⅱ向B中加入稀硫酸,出现白色沉淀,继续滴加稀硫酸至过量,白色沉淀完全溶解,说明溶液B只有NaAlO2溶液,没有硅酸钠,则推断固体样品不含二氧化硅;
故答案为:SiO2;
(3)因为Cu2O+2H+═Cu+Cu2++H2O,向A中加入足量稀硫酸并微热,完全溶解,则必定含Fe3O4与硫酸反应生成三价铁,将生成的单质铜氧化成铜离子而全部溶解,所以溶液C必定含过量的氢离子、二价铁、二价铜的混合溶液可能还含有三价铁;所以在含有三价铁的溶液中检验二价铁一般用酸性KMnO4溶液,看是否退色;故答案为:Fe2+;向酸性KMnO4溶液中滴加待测液,褪色.
(4)根据氢氧化物在溶液中沉淀的pH表,Ⅳ中加NaClO的目的是将Fe2+氧化成Fe3+,增大溶液的pH使Fe3+生成Fe(OH)3沉淀,故答案为:将Fe2+氧化成Fe3+,增大溶液的pH使Fe3+生成Fe(OH)3沉淀;
(5)根据以上分析可能的组合为:组合1:Al、Fe2O3、Cu2O;组合2:Al、Cu2O、Fe3O4;组合3:Al、Fe2O3、Cu2O、Fe3O4.故答案为:Al、Fe2O3、Cu2O;Al、Cu2O、Fe3O4(Al、Fe2O3、Cu2O、Fe3O4).
点评 本题考查了物质检验方法的应用,物质性质的分析判断,主要是物质检验的方法和现象应用,化学方程式的书写方法,物质检验的方案设计,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1.00 mol•L-1 | B. | 0.500 mol•L-1 | C. | 2.00 mol•L-1 | D. | 3.00 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 气体1可能为NO和CO2的混合物 | |
| B. | 沉淀3可能为Mg(OH)2和Al(OH)3的混合物 | |
| C. | 沉淀4可能为BaCO3、BaSO3或二者混合物 | |
| D. | 固体粉末X中一定有Na2CO3,可能有KAlO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 熔融态的A中阴离子有2种 | |
| B. | C溶于水会促进水的电离 | |
| C. | 将A溶液滴入B溶液中,能使B溶液中阳离子浓度增大 | |
| D. | B溶液的焰色反应呈黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
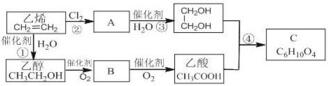
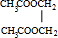 +2H2O.
+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com