
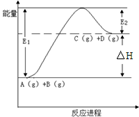
| A. | 该反应是放热反应 | |
| B. | 加入催化剂后,反应加快,△H减小 | |
| C. | 反应物的总键能小于生成物的总键能 | |
| D. | 反应达到平衡时,升高温度,A的转化率增大 |
分析 A.依据反应物和生成物能量变化判断反应为吸热反应;
B.图中△H为该反应的热效应,加催化剂无影响;
C.反应物断键吸收能量和生成物成键放出能量;
D.根据温度对平衡的影响分析.
解答 解:A.由图可知,该反应的反应物的总能量小于生成物的总能量,所以反应为吸热反应,故A错误;
B.图中△H为该反应的热效应,加催化剂,降低了反应所需的活化能,但是反应热不变,即催化剂对△E无影响,故B错误;
C.反应物断键吸收能量和生成物成键放出能量,该反应为吸热反应,所以反应物断键吸收能量大于生成物成键放出能量,故C错误;
D.该反应为吸热反应,所以反应达到平衡时,升高温度,平衡正移,则A的转化率增大,故D正确;
故选D.
点评 本题考查了反应焓变的判断,图象分析是关键,催化剂的作用分析是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | O2- Na+Mg2+Al3+ | B. | O Cl S P | ||
| C. | K+ Mg2+ Al3+ H+ | D. | A l3+Mg2+ Ca2+ F- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 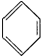 +HNO3$→_{55-60℃}^{浓H_{2}SO_{4}}$ +HNO3$→_{55-60℃}^{浓H_{2}SO_{4}}$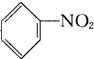 +H2O +H2O | B. | CH2═CH2+H2$\stackrel{催化剂}{→}$CH3-CH3 | ||
| C. | CH3-CH3+Cl2$\stackrel{光照}{→}$CH3-CH2Cl+HCl | D. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
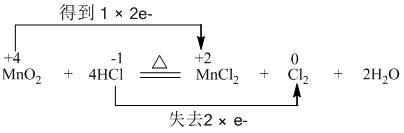
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C4H6 | B. | C2H6 | C. | C6H6 | D. | C4H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | XY | B. | Y2X | C. | Y2X2 | D. | Y3X2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | |||
| z | W | Q |
| A. | Y元素气态氢化物的稳定性大于X元素的气态氢化物 | |
| B. | 形成的简单离子半径:W>Q>Z>X | |
| C. | Q的最高价氧化物对应的水化物酸性最强 | |
| D. | X的最高价氧化物对应的水化物与其氢化物形成的化合物中含有离子键和共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com