

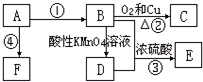
| A、试剂X可以是氢氧化钠溶液,也可以是盐酸 |
| B、反应①过滤后所得沉淀为氢氧化铁 |
| C、反应②通入的过量Y是CO2气体 |
| D、图中所示的转化反应①②都是氧化还原反应 |


科目:高中化学 来源: 题型:

| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯通过缩聚反应形成聚乙烯 |
| B、石油产品都可用于聚合反应 |
| C、淀粉、纤维素都属于高分子化合物 |
| D、聚丙烯的结构简式为?CH2-CH2-CH2? |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、非金属气态氧化物都不是电解质 |
| B、SO2、NO2、C02都会导致酸雨的形成 |
| C、氮的氧化物都属于大气污染物 |
| D、Si、S的氧化物均属于酸性氧化物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com