
已知在800 K时,反应:CO(g)+H2O(g)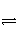
 H2(g)+CO2(g),若初始浓度c0(CO)=2 mol·L-1,c0(H2O)=3 mol·L-1,则反应达到平衡时,CO转化成CO2的转化率为60%,如果将H2O的初始浓度加大为6 mol·L-1,试求此时CO转化为CO2的转化率。
H2(g)+CO2(g),若初始浓度c0(CO)=2 mol·L-1,c0(H2O)=3 mol·L-1,则反应达到平衡时,CO转化成CO2的转化率为60%,如果将H2O的初始浓度加大为6 mol·L-1,试求此时CO转化为CO2的转化率。
此时CO转化为CO2的转化率为75%。
解析 (1)平衡转化率与平衡常数不同,它受到反应物初始浓度的影响。
(2)平衡转化率的数学表达式是涉及平衡转化率计算的基本依据。
由第一次平衡时CO的转化率可求出平衡时各物质的浓度:[CO]=0.8 mol·L-1,[H2O]=1.8 mol·L-1,[H2]=1.2 mol·L-1,[CO2]=1.2 mol·L-1,K=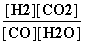 =
=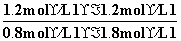 =1,假设第二次平衡时,CO的转化浓度为x。
=1,假设第二次平衡时,CO的转化浓度为x。
CO(g)+H2O(g)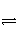
 H2(g)+CO2(g)
H2(g)+CO2(g)
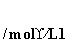 2 6 0 0
2 6 0 0
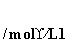 2-x 6-x x x
2-x 6-x x x
则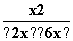 =1,解得x=1.5 mol·L-1,故CO的转化率为
=1,解得x=1.5 mol·L-1,故CO的转化率为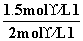 ×100%=75%。
×100%=75%。


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:
下列叙述正确的是 ( )
含金属元素的离子一定都是阳离子
在氧化还原反应中,非金属单质一定是氧化剂
C. 某元素从游离态变为化合态时,该元素一定被还原
D.金属阳离子被还原不一定得到金属单质
查看答案和解析>>
科目:高中化学 来源: 题型:
1)向NaHSO4溶 液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式
液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式 :_________________________________________________
:_________________________________________________ ______。
______。
(2)向Ba(OH)2溶液中逐滴加入NaHSO4溶液至恰好不再生成沉淀时为止,请写出发生反应的离子方程式:____________________________________________。
(3)向Ba(OH)2溶液中逐 滴加入明矾[KAl(SO4)2·12H2O]至溶液中Ba2+恰好完全沉淀,反应的离子方程式是:_________________________________________。
滴加入明矾[KAl(SO4)2·12H2O]至溶液中Ba2+恰好完全沉淀,反应的离子方程式是:_________________________________________。
在以上溶液中 继续滴加明矾溶液,请写出此步反应的离子方程式:_________。
继续滴加明矾溶液,请写出此步反应的离子方程式:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在一定条件下2SO2(g)+O2(g)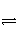
 2SO3(g) ΔH=-Q kJ·mol-1。向一密闭容器中加入2 mol SO2和1 mol O2,达平衡时SO2的转化率为90%,放出的热量为Q1;向另一相同容器中加入2 mol SO3,在相同条件下,达平衡时吸收的热量为Q2,则下列关系中正确的是( )
2SO3(g) ΔH=-Q kJ·mol-1。向一密闭容器中加入2 mol SO2和1 mol O2,达平衡时SO2的转化率为90%,放出的热量为Q1;向另一相同容器中加入2 mol SO3,在相同条件下,达平衡时吸收的热量为Q2,则下列关系中正确的是( )
A.Q>Q1>Q2 B.Q1>Q2>Q C.Q1>Q>Q2 D.Q1=Q2>Q
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g)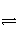
 1/2N2(g)+CO2(g) ΔH=-373.2 kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
1/2N2(g)+CO2(g) ΔH=-373.2 kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
A.加催化剂同时升高温度
B.加催化剂同时增大压强
C.升高温度同时充入N2
D.降低温度同时增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g)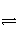
 nY(g) ΔH=Q kJ·mol-1。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
nY(g) ΔH=Q kJ·mol-1。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:

下列说法正确的是( )
A.m>n
B.Q<0
C.温度不变,压强增大,Y的质量分数减少
D.体积不变,温度升高,平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
取五等份NO2 ,分别加入温度不同、容积相同的恒容密闭容器中,发生反应:
2NO2(g)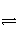
 N2O4(g) ΔH<0
N2O4(g) ΔH<0
反应相同时间后,分别测定体系中NO2的百分含量(NO2%),并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是( )
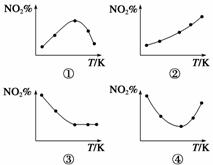
A.①② B.①④ C.②③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在室温的条件下,pH均为5的H2SO4溶液和NH4Cl溶液,回答下列问题:
(1)各取5mL上述溶液,分别加水稀释至50mL,pH较大的是________溶液
(2)各取5mL上述溶液,分别加热(温度相同),pH较小的是________溶液
(3)H2SO4溶液和NH4Cl溶液中由水电离出的c(H+)之比为__________
(4)取5mL NH4Cl溶液,加水稀释至50mL,c(H+) ____________ 10-6mol·L-1(填“>”、“<”或“=”),c(NH4+)/c(H+)_______________(填“增大”、“减小”或“不变”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com