
【题目】向含有Na2CO3、NaAlO2的混合溶液中逐滴加入150 mL 1 mol L-1的HC1溶液,测得溶液中某几种离子的物质的量的变化情况如图所示。下列说法不正确的是
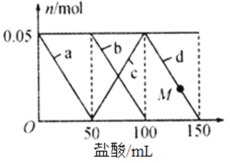
A.b和c曲线表示的离子反应均为CO32-+H+= HCO3-
B.结合H+的能力:AlO2>CO32> HCO3>Al(OH)3
C.原混合溶液中,CO32与AlO2的物质的量之比为2∶1
D.M点时A1(OH)3的质量等于3.9 g
【答案】C
【解析】
向Na2CO3、NaAlO2的混合溶液中逐滴加入150mL1molL-1的盐酸,先发生反应AlO2-+H++H2O═Al(OH)3↓,a线表示AlO2-减少,第二阶段,AlO2-反应完毕,发生反应CO32-+H+═HCO3-,b线表示CO32-减少,c线表示HCO3-的增加,第三阶段,CO32-反应完毕,发生反应HCO3-+H+═CO2↑+H2O,d线表示HCO3-减少,此阶段Al(OH)3不参与反应,据此结合选项解答。
A.b曲线表示碳酸钠和盐酸反应,c曲线也表示碳酸钠和盐酸的反应,只是b曲线表示碳酸钠的物质的量,c曲线表示碳酸氢钠的物质的量,所以b和c曲线表示的离子反应是相同的,都是CO32+H+═HCO3,故A正确;
B.根据以上分析,氢离子先与A1O2反应,再与CO32反应,后与HCO3反应,最后才溶解Al(OH)3,所以结合H+的能力:A1O2>CO32>HCO3>Al(OH)3,故B正确;
C.由图象知,Na2CO3、NaAlO2的物质的量相等都是0.05mol,由此判断溶液中CO32与AlO2的物质的量之比为1:1,故C错误;
D.盐酸50mL时NaAlO2中铝元素全部转化为氢氧化铝沉淀,加50mL盐酸之后CO32-反应,氢氧化铝沉淀不溶解,则M点沉淀的质量和盐酸50mL时沉淀的质量相同,由NaAlO2+HCl+H2O=NaCl+Al(OH)3↓可知,n(Al(OH)3)=n(NaAlO2)=n(HCl)=0.05mol,m(Al(OH)3)=0.05mol×78g/mol=3.9g,故D正确;
答案选C。


科目:高中化学 来源: 题型:
【题目】已知某些共价键的键能如表所示,试回答下列问题:℃
共价键 | 键能 | 共价键 | 键能 |
| 436 |
| 467 |
| 243 |
| 945 |
| 413 |
| 431 |
(1)![]() 键的键能为什么比
键的键能为什么比![]() 键的键能大_______?
键的键能大_______?
(2)已知![]() 在
在![]() 时有
时有![]() 的分子分解,而
的分子分解,而![]() 在
在![]() 时可能完全分解为
时可能完全分解为![]() 和
和![]() ,试解释其中的原因_______。
,试解释其中的原因_______。
(3)试解释氮气能在空气中稳定存在的原因_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧乙酸(CH3COOOH)是一种高效消毒剂,性质不稳定遇热易分解,可利用高浓度的双氧水和冰醋酸反应制得,某实验小组利用该原理在实验室中合成少量过氧乙酸。装置如图所示。回答下列问题:
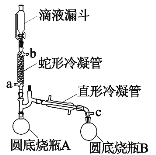
已知:①常压下过氧化氢和水的沸点分别是158℃和100℃。
②过氧化氢易分解,温度升高会加速分解。
③双氧水和冰醋酸反应放出大量的热。
(1)双氧水的提浓:蛇形冷凝管连接恒温水槽,维持冷凝管中的水温为60℃,c口接抽气泵,使装置中的压强低于常压,将滴液漏斗中低浓度的双氧水(质量分数为30%)滴入蛇形冷凝管中。
①蛇形冷凝管的进水口为___________。
②向蛇形冷凝管中通入60℃水的主要目的是________。
③高浓度的过氧化氢最终主要收集在______________(填圆底烧瓶A/圆底烧瓶B)。
(2)过氧乙酸的制备:向100mL的三颈烧瓶中加入25mL冰醋酸,滴加提浓的双氧水12mL,之后加入浓硫酸1mL,维持反应温度为40℃,磁力搅拌4h后,室温静置12h。
①向冰醋酸中滴加提浓的双氧水要有冷却措施,其主要原因是__________。
②磁力搅拌4h的目的是____________。
(3)取V1mL制得的过氧乙酸溶液稀释为100mL,取出5.0mL,滴加酸性高锰酸钾溶液至溶液恰好为浅红色(除残留H2O2),然后加入足量的KI溶液和几滴指示剂,最后用0.1000mol/L的Na2S2O3溶液滴定至终点,消耗标准溶液V2mL(已知:过氧乙酸能将KI氧化为I2;2Na2S2O3+I2=Na2S4O6+2NaI)。
①滴定时所选指示剂为_____________,滴定终点时的现象为___________。
②过氧乙酸与碘化钾溶液反应的离子方程式为_________。
③制得过氧乙酸的浓度为________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将 0.10 mol·L-1 盐酸滴入 20.00 mL 0.10 mol·L-1 氨水中,溶液中 pH 和 pOH 随加入盐酸体积变化曲线如图所示。已知:pOH=—lgc(OH),下列正确的是
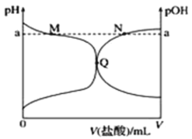
A.M 点所示溶液中可能存在:c(Cl)>c(NH4+)
B.M 点到Q点所示溶液中水的电离程度先变大后减小
C.Q 点盐酸与氨水恰好中和
D.N 点所示溶液中可能存在:c(NH4+)+c(NH3·H2O)=c(Cl)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。
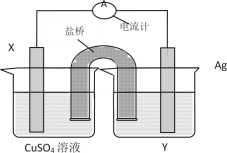
请回答下列问题:
(1)电解质溶液Y是__;
(2)X电极上发生的电极反应为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向20mL0.1mol/LH2R溶液中滴加0.1mol/LNaOH溶液,溶液的pH随NaOH溶液体积的变化如图所示。已知pKa = –lgKa,二元弱酸H2R的pKa1=1.89,pKa2=7.21.下列有关说法错误的是
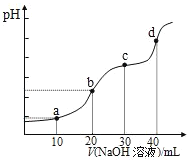
A.H2R + R22HR平衡常数K>105,反应趋于完全
B.常温下,Kh(HR-)的数量级为10-13
C.点b时,pH<7且 c(R2)·c(H+)<c(H2R)·c(OH)
D.点c时,溶液中2c(OH)-2c(H+)=3c(H2R)+ c(HR)-c(R2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据原子结构、元素周期表和元素周期律的知识回答下列问题:
(1)A元素次外层电子数是最外层电子数的![]() ,其外围电子的轨道表示式是 ________ 。
,其外围电子的轨道表示式是 ________ 。
(2)B是1~36号元素原子核外电子排布中未成对电子数最多的元素,B元素的名称是 _______ ,在元素周期表中的位置是 _______ 。
(3)C元素基态原子的轨道表示式是下图中的 ____________ (填序号),另一轨道表示式不能作为基态原子的轨道表示式是因为它不符合 ____________ (填序号)。
①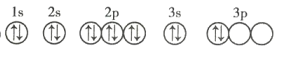
②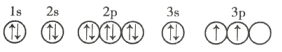
A 能量最低原则 B 泡利不相容原理 C 洪特规则
(4)元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能a叫作第一电离能(设为E)。第三周期元素的第一电离能示意图如图所示:
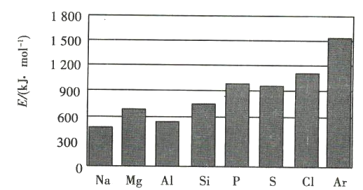
①同周期内,随着原子序数的增大,E值变化的总趋势是 ____________ ;
②根据图中提供的信息,可推断出E氧 ______ E氟(填“>”“<”或“=”,下同);
③根据第一电离能的含义和元素周期律,可推断出E镁 ____________ E钙。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表前四周期的一部分,下列有关X、Y、Z、R、W五种元素的叙述中,错误的是
X | ||||
Y | Z | |||
R | W |
A.常压下五种元素的单质中,Y的沸点最高
B.元素电负性:X>Z>Y
C.基态原子中未成对电子数最多的是R
D.元素最高价氧化物对应的水化物酸性:W>Z>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有前四周期的5种元素的部分信息如下表所示:
元素代号 | 元素部分信息 |
X | X的阴离子核外电子云均呈球形 |
Y | 原子的最高能级上有3个未成对电子,其最简单气态氢化物在水中的溶解度在同族元素所形成的最简单气态氢化物中最大 |
Z | 基态原子核外有3个能级填充了电子,能量最高能级的电子数等于前两个能级的电子数之和 |
R | 元素原子的最外层电子排布式为nsn-1npn-1 |
T | 一种核素的质量数为65,中子数为36 |
根据上述元素信息,回答下列问题。
(1)基态T2+的电子排布式为__。
(2)Y、Z、R的电负性由大到小的顺序为__(用元素符号表示)。
(3)YX4+的空间构型为__,离子中![]() 原子的杂化轨道类型为___,YX4+的电子式为__。
原子的杂化轨道类型为___,YX4+的电子式为__。
(4)YX3的一种等电子体分子是__,YX3的键角大于X2Z的键角的主要原因是__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com