
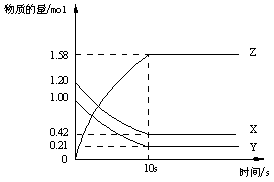
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:
下列描述正确的是( )
A.反应开始到10s,用Z表示的反应速率为0.158mol/(Ls)
B.反应开始到10s,X的物质的量浓度减少了0.79mol/L
C.反应开始到10s时,Y的转化率为79.0%
 D.反应的化学方程式为: X(g)+Y(g)
D.反应的化学方程式为: X(g)+Y(g)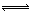 Z(g)
Z(g)
科目:高中化学 来源: 题型:
元素周期表是一座开放的“元素大厦”,元素大厦尚未充满。若发现119号元素,请您在元素大厦中安排好它的“房间” ( )
A.第七周期第0族 B.第六周期ⅡA族 C.第八周期第ⅠA族 D.第七周期第ⅦA族
查看答案和解析>>
科目:高中化学 来源: 题型:
已知次氯酸是比碳酸还弱的酸,反应Cl2 + H2O 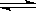 HCl + HClO达平衡后,要使HClO浓度增大,可加入( )
HCl + HClO达平衡后,要使HClO浓度增大,可加入( )
A.6mol/L NaOH溶液 B.6mol/L H2SO4溶液
C.CH3COONa固体 D.Na2SO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
已知热化学方程式:
H2O(g)=H2(g) + 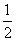 O2(g) △H = +241.8kJ/mol
O2(g) △H = +241.8kJ/mol
H2(g)+ 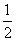 O2(g) = H2O(1) △H = -285.8kJ/mol
O2(g) = H2O(1) △H = -285.8kJ/mol
当1g液态水变为水蒸气时,其热量变化是( )
A.吸热88kJ B. 吸热2.44kJ
C.放热44kJ D. 吸热44kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
有关碰撞理论,下列说法中不正确的是( )
A.具有足够能量的分子(活化分子)相互碰撞就一定能发生化学反应
B.增大反应物浓度,单位体积内活化分子数增多,有效碰撞的几率增大,反应速率增大
C.升高温度,活化分子百分数增大,有效碰撞的几率增大,反应速率增大
D.正催化剂能降低反应的活化能,提高活化分子百分数,有效碰撞的几率增大,反应速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
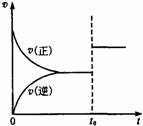
可逆反应aX(g)+bY(g)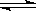 cZ(g),在一定温度下的密闭容器内达到平衡后,t0时改变某一外界条件,化学反应速率(v)和时间(t)的关系如下图所示。下列说法中正确的是( )
cZ(g),在一定温度下的密闭容器内达到平衡后,t0时改变某一外界条件,化学反应速率(v)和时间(t)的关系如下图所示。下列说法中正确的是( )
A.若a+b=c,则t0时只增大了反应物的浓度
B.若a+b=c,则t0时只升高了温度
C.若a+b≠c,则t0时只增大了容器的压强
D.若a+b≠c,则t0时只加入了催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
在10L容器中,加入2mol的SO2(g)和2mol的NO2(g),保持温度恒定,发生反应:
SO2(g)+ NO2(g) 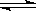 SO3(g)+NO(g)。当达到平衡状态时,测得容器中SO2(g)的转化率为50%。
SO3(g)+NO(g)。当达到平衡状态时,测得容器中SO2(g)的转化率为50%。
试求:该温度下、该容器中,再继续加入1mol的SO2(g),则:
(1)化学平衡将向________方向移动,NO2的转化率将____________;
(2)经计算,当达到新的平衡状态时,容器中SO2(g)的浓度是_______mol/L;
(3)整个过程中,SO2的转化率由50%变为_______%,NO2的转化率由__________%变为_______%。
(4)计算结果给我们的启示是:增大一种反应物物的用量,其转化率将________________(填“增大” 、“不变”或“减小”)另一反应物的转化率将____________(填“增大” 、“不变”或“减小”)。现实生产中的意义是:可以通过增大________的用量,来提高成本高的反应物的利用率。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于有机物的说法正确的是
A.乙烯和聚乙烯都能使溴的四氯化碳溶液褪色
B.甲烷、乙烯和苯都能与酸性高锰酸钾溶液反应
C.乙酸乙酯和油脂在一定条件下都能水解
D.所有烷烃中都存在碳碳单键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com