
【题目】某 500 mL 溶液中只可能含有 Na+、NH4+、Mg2+、Al3+、Fe2+、Fe3+、Cl-、![]() 、
、![]() 中 的几种离子。
中 的几种离子。
已知:NH4++OH-=NH3↑ +H2O
(1)取该溶液l00 mL,逐滴加入足量的NaOH溶液并加热,生成标准状况下的气体体积为 896 mL(气体已全部逸出),滴加过程中无沉淀生成。则该溶液中一定不含有的阳离子是______.
(2)另取100 mL原溶液于试管中,滴加足量的BaCl2溶液,生成白色沉淀6.27 g,再加入足量稀盐酸,沉淀部分溶解,生成标准状况下的气体体积为448 mL。则原浓液中下列离子的浓度:
离子种类 | 离子浓度 |
| ①___molL-1 |
| ②___ molL-1 |
Na+ | ③__molL-1 |
写出加入盐酸时,生成气体的离子方程式:__________。
【答案】Al3+、Fe2+、Fe3+、Mg2+ 0.2 0.1 0.2 BaCO3+2H+ = Ba2+ +H2O+CO2 ↑
【解析】
![]() 取100mL该溶液,逐滴加入足量NaOH溶液,在整个滴加过程中无沉淀生成,
取100mL该溶液,逐滴加入足量NaOH溶液,在整个滴加过程中无沉淀生成,![]() 、
、![]() 、
、![]() 、
、![]() 能与碱反应产生沉淀,说明溶液中肯定不含有
能与碱反应产生沉淀,说明溶液中肯定不含有![]() 、
、![]() 、
、![]() 、
、![]() ;
;![]() 另取100mL原溶液于试管中,滴加足量氯化钡溶液,生成白色沉淀
另取100mL原溶液于试管中,滴加足量氯化钡溶液,生成白色沉淀![]() ,再加入足量稀盐酸,沉淀部分溶解,说明有
,再加入足量稀盐酸,沉淀部分溶解,说明有![]() 和
和![]() ,标准状况下的气体为
,标准状况下的气体为![]() ,即
,即![]() ,根据碳原子守恒有:
,根据碳原子守恒有:![]() ,碳酸钡质量
,碳酸钡质量![]() 克,硫酸钡质量
克,硫酸钡质量![]() 克,即
克,即![]() 。根据加入足量的NaOH溶液并加热,生成标准状况下的气体体积为896mL,知道含
。根据加入足量的NaOH溶液并加热,生成标准状况下的气体体积为896mL,知道含![]() ,根据
,根据![]() 求浓度,根据电荷守恒判断是否含有钠离子,碳酸钡与盐酸反应生成氯化钡、二氧化碳与水,据此答题。
求浓度,根据电荷守恒判断是否含有钠离子,碳酸钡与盐酸反应生成氯化钡、二氧化碳与水,据此答题。
![]() 取100mL该溶液,逐滴加入足量NaOH溶液,在整个滴加过程中无沉淀生成,
取100mL该溶液,逐滴加入足量NaOH溶液,在整个滴加过程中无沉淀生成,![]() 、
、![]() 、
、![]() 、
、![]() 能与碱反应产生沉淀,说明溶液中肯定不含有
能与碱反应产生沉淀,说明溶液中肯定不含有![]() 、
、![]() 、
、![]() 、
、![]() ,故答案为:
,故答案为:![]() 、
、![]() 、
、![]() 、
、![]() ;
;
![]() 另取100ml原溶液于试管中,滴加足量氯化钡溶液,生成白色沉淀
另取100ml原溶液于试管中,滴加足量氯化钡溶液,生成白色沉淀![]() ,再加入足量稀盐酸,沉淀部分溶解,说明有
,再加入足量稀盐酸,沉淀部分溶解,说明有![]() 和
和![]() ,标准状况下的气体为
,标准状况下的气体为![]() ,即
,即![]() ,
,![]() ,碳酸钡质量
,碳酸钡质量![]() 克,硫酸钡质量
克,硫酸钡质量![]() 克,为
克,为![]() ,根据
,根据![]() ,可得:
,可得:![]() ,
,![]() ,据加入足量的NaOH溶液并加热,生成标准状况下的气体体积为896mL,知道含
,据加入足量的NaOH溶液并加热,生成标准状况下的气体体积为896mL,知道含![]() ,
,![]() ,题中没有信息说明无氯离子,故根据电荷守恒,
,题中没有信息说明无氯离子,故根据电荷守恒,![]() ,将浓度数值代入得
,将浓度数值代入得![]() ,碳酸钡与盐酸反应生成氯化钡、二氧化碳与水,反应离子方程式为
,碳酸钡与盐酸反应生成氯化钡、二氧化碳与水,反应离子方程式为![]() ,故答案为:
,故答案为:![]() ;
;![]() ;
;![]() ;
;![]() 。
。


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案科目:高中化学 来源: 题型:
【题目】化学上常用AG表示溶液中的lg![]() 。25℃时,用0.100molL-1的NaOH溶液滴定20.00mL 0.100molL-1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )
。25℃时,用0.100molL-1的NaOH溶液滴定20.00mL 0.100molL-1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )
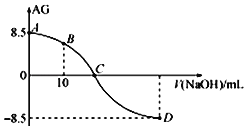
A. D点溶液的pH=11.25
B. C点之前溶液显碱性,C点之后溶液显酸性
C. C点时,加入NaOH溶液的体积为20mL
D. 25℃时,HNO2的电离常数Ka=1.0×10-5.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列叙述正确的是
A.5. 6 L由CO2和O2组成的混合气体中的分子数为0. 25NA
B.5. 6 g铁与足量的稀硫酸完全反应转移的电子数为0. 2NA
C.0. 5 mol L-1的BaCl2溶液中含有Cl-的数目为NA
D.10 g质量分数为17%的H2O2溶液中含氧原子的数目为0. 1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组对甲酸进行了如下的实验,以验证其含有醛基,并考察其化学性质。首先做了银镜反应:
(1)取少量甲酸加入NaOH溶液中和其酸性,反应的离子方程式为_________________。
(2)在(1)的溶液中加入足量银氨溶液,加热,产生了银镜。甲酸钠溶液与银氨溶液发生银镜反应的离子方程式为_______________________________________________。
(3)某同学很成功的做了银镜反应,他肯定没有进行的操作_________________(写字母):
A.用洁净的试管 B.向银氨溶液中加入硝酸酸化
C.用前几天配制好的银氨溶液 D.直接在银氨溶液里加入稍过量的甲酸;
E.在浓度为2%的NH3H2O中滴入稍过量的浓度为2%的硝酸银
然后,同学们对甲酸与甲醇的酯化反应进行了研究:
(4)写出![]() 和CH3-18OH进行酯化反应的化学方程式______________________。
和CH3-18OH进行酯化反应的化学方程式______________________。
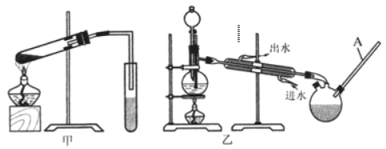
(5)你认为选择甲装置还是乙装置好?_______,原因是______________________。乙装置中长导管C的作用是_________________。
(6)实验中饱和碳酸钠溶液的作用是_____________________________。从饱和碳酸钠溶液中分离出酯需要用到的主要实验仪器是_______________。
(7)一同学用装有饱和氢氧化钠的三颈烧瓶接收甲酸甲酯,几乎没有收集到产物,请给予合理的解释_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水杨酸冬青油、阿司匹林的结构简式如图,下列说法不正确的是
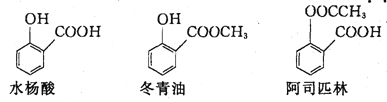
A. 由水杨酸制冬青油的反应是取代反应
B. 阿司匹林的分子式为C9H8O4,在一定条件下水解可得水杨酸
C. 冬青油苯环上的一氯取代物有4种
D. 可用NaOH溶液除去冬青油中少量的水杨酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知298K时下列物质的溶度积
CH3COOAg | AgCl | AgCrO4 | AgS | |
Ksp | 2.3×10-3 | 1.77×10-10 | 1.12×10-12 | 6.7×10-15 |
下列说法正确的是( )
A.等体积浓度均为0.02molL-1的CH3COONa和AgNO3溶液混合能产生沉淀
B.浓度均为0.01molL-1的CrO42-和Cl-混合溶液中慢慢滴入AgNO3溶液时,CrO42-先沉淀
C.在CH3COOAg悬浊液中加入盐酸发生反应的离子方程式:CH3COOAg+H++C1-=CH3COOH+AgCl
D.298K时,上述四种饱和溶液的物质的量浓度:c(CH3COOAg)>c(AgCl)>c(Ag2CrO4)>c(Ag2S)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为消除目前燃料燃烧时产生的环境污染,同时缓解能源危机,有关专家提出了利用太阳能制取氢能的构想。下列说法正确的是
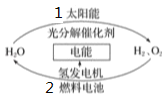
A. 过程1是放热反应
B. 过程2可将化学能转化为电能
C. 氢能源可从自然界直接获取,是一次能源
D. 氢气不易贮存和运输,无开发利用价值
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计实验探究构成原电池的条件,装置如图所示:
甲. 乙.
乙.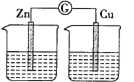
实验一:探究电极的构成。图甲中,①A、B两极均选用石墨作电极,发现电流计指针不偏转;②A、B两极均选用铜片作电极,发现电流计指针不偏转;③A极用锌片,B极用铜片,发现电流计指针向左偏转;④A极用锌片,B极用石墨,发现电流计指针向左偏转。
(1)结论一:________________________;
实验二:探究溶液的构成。图甲中,A极用锌片,B极用铜片,①液体采用无水乙醇,发现电流计指针不偏转;②改用硫酸溶液,发现电流计指针偏转,B极上有气体产生。
(2)结论二:________________________;
实验三:探究图乙装置能否构成原电池。将锌、铜两电极分别放入稀硫酸中,发现锌片上有气泡产生,铜片上无明显现象,电流计指针不发生偏转。
(3)结论三:________________________;
思考:对该同学的实验,有同学提出了如下疑问,请你帮助解决。
(4)在图甲装置中,若A为镁片,B为铝片,电解质溶液为![]() 溶液;负极为________(填“A”或“B”);电流计的指针应向________(填“右”或“左”)偏转。
溶液;负极为________(填“A”或“B”);电流计的指针应向________(填“右”或“左”)偏转。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国劳伦斯·利弗摩尔国家实验室(LLNL)设计的以熔融的碳酸盐为电解液,泡沫镍为电极,氧化纤维布为隔膜的直接碳燃料电池结构如图所示,下列说法错误的是( )
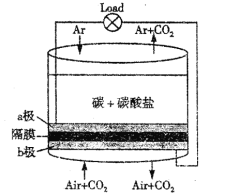
A. a极通气的目的是增强导电能力
B. a极的电极反应式为C+2CO32--4e-=3CO2↑
C. 电流由b极沿导线经负载再流向a极
D. CO32-由b极区透过隔膜流向a极区
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com