
| A. | 甲烷分子的球棍模型: | B. | NH4Cl的电子式: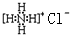 | ||
| C. | F原子的结构示意图: | D. | 中子数为20的氯原子${\;}_{17}^{37}$Cl |
分析 A、甲烷中的H原子半径小于碳原子的半径;
B、氯化铵为离子化合物,由铵根离子和氯离子构成;
C、原子结构示意图中,原子核带正电;
D、质量数=质子数+中子数.
解答 解:A.甲烷分子的球棍模型中应中间的为C,且C原子半径比H原子半径大,故正确的应为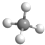 ,故A错误;
,故A错误;
B.氯化铵是离子化合物,由铵根离子和氯离子构成,电子式为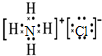 ,故B错误;
,故B错误;
C.原子结构示意图中,原子核带正电,故F的原子结构示意图为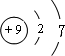 ,故C错误;
,故C错误;
D.质量数=质子数+中子数,故中子数为20的氯原子为3717Cl,故D正确;
故选D.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及球棍模型、电子式、元素符号等知识,试题知识点较多,充分考查了学生规范答题的能力,注意熟练掌握常见化学用语的概念及书写原则.


 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:选择题
| A. | 增大反应物的量,化学反应速率一定加快 | |
| B. | 气体反应体系的压强增大,化学反应速率一定加快 | |
| C. | 与金属锌反应时,硫酸的浓度越大,产生H2速率越快 | |
| D. | 2molX气体在2L的容器中反应,4s后浓度变为0.5mol•L-1,则其反应速率为0.125mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
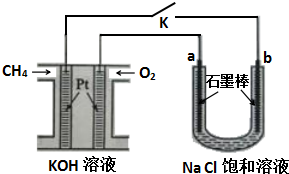
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2(g)+Cl2(g)═$\frac{1}{2}$HCl(g)△H=+92.4kJ/mol | B. | H2(g)+Cl2(g)═$\frac{1}{2}$HCl(g)△H=-92.4kJ/mol | ||
| C. | H2(g)+Cl2(g)═2HCl(g)△H=-184.8kJ/mol | D. | H2(g)+Cl2(g)═2HCl(l)△H=+184.8kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①②③ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 物质 | 用途 | 解释 |
| A | H2O2 | 消毒剂 | H2O2具有强氧化性,可杀菌 |
| B | SiO2 | 计算机芯片 | SiO2是一种良好的半导体 |
| C | Fe3O4 | 红色涂料 | Fe3O4是一种红色氧化物 |
| D | 浓H2SO4 | 干燥剂 | 浓H2SO4有脱水性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
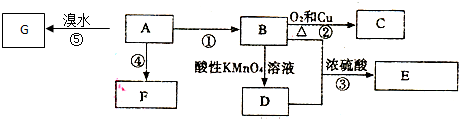
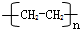 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com