
| A. | ③④⑤⑧ | B. | ③⑥⑦ | C. | ③⑥⑦⑧ | D. | ②④⑤⑥⑦⑧ |
分析 元素的非金属性越强,其得电子能力越强,氯元素原子得电子能力比硫强,说明Cl元素的非金属性比S元素强,可以根据其氢化物的稳定性、其单质的氧化性、其单质与氢气化合难易程度、其最高价氧化物的水化物酸性强弱判断,据此分析解答.
解答 解:元素的非金属性越强,其得电子能力越强,氯元素原子得电子能力比硫强,说明Cl元素的非金属性比S元素强,
①HCl的溶解度比H2S大与其非金属性强弱无关,故错误;
②HCl的酸性比H2S强,说明HCl电离程度大于硫化氢,与其非金属性强弱无关,故错误;
③元素的非金属性越强,其氢化物的稳定性越强,HCl的稳定性比H2S强,说明Cl元素得电子能力大于S,故正确;
④元素的非金属性越强,其简单阴离子的还原性越弱,HCl的还原性比H2S弱,故错误;
⑤HClO的酸性较弱,硫酸是强酸,所以次氯酸的酸性比H2SO4弱,故错误;
⑥Cl2能与H2S反应生成S,说明氯气氧化性大于S,则得电子能力Cl大于S,故正确;
⑦Cl2与铁反应生成FeCl3,而S与铁反应生成FeS,说明氯气氧化性大于S,则得电子能力Cl大于S,故正确;
⑧元素的非金属性越强,其简单阴离子的还原性越弱,还原性:Cl-<S2-,说明非金属性Cl>S,则得电子能力Cl>S,故正确;
故选C.
点评 本题考查非金属性强弱判断方法,为高频考点,侧重考查学生对知识的灵活运用能力,非金属性强弱与得电子多少无关,与得电子难易程度有关,题目难度不大.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:解答题
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅰ | x≥a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| Ⅱ | a>x≥b | 电极附近出现黄色,无气泡产生 | 有Fe3+、无Cl2 |
| Ⅲ | b>x>0 | 无明显变化 | 无Fe3+、无Cl2 |
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅳ | a>x≥c | 无明显变化 | 有Cl2 |
| Ⅴ | c>x≥b | 无明显变化 | 无Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
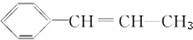 ,它可能具有的性质是( )
,它可能具有的性质是( )| A. | 易溶于水也易溶于有机溶剂 | |
| B. | 能发生加聚反应,其生成物可用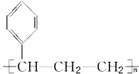 表示 表示 | |
| C. | 能使溴水褪色,但不能使酸性KMnO4溶液褪色 | |
| D. | 既能使溴水褪色,又能使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:B>A>C>D | B. | 原子序数:d>c>b>a | ||
| C. | 离子半径:D ->C 2->B +>A 2+ | D. | 离子的还原性:D ->C 2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C与浓HNO3反应 | B. | Cu与浓HNO3反应 | C. | Cu与稀HNO3反应 | D. | Mg(OH)2与HNO3反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,4.6gHCOOH和C2H5OH的混合物的分子总数为0.1NA | |
| B. | 标准状况下,11.2LNO和O2的混合气体含有的原子总数为1.5NA | |
| C. | 2L0.5mol/L的AlCl3溶液中,含有离子总数为4NA | |
| D. | 常温下,56gFe与足量的浓硝酸反应,转移电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2gH2的分子数为NA | |
| B. | 标准状况下,22.4LH2O含有NA个水分子 | |
| C. | 5.6g铁与足量盐酸反应转移的电子数为0.3NA | |
| D. | 1mol/LMg(NO3)2溶液中含有NO3-的数目为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com