
| A. | 滴入NaOH溶液,产生白色沉淀,则原溶液一定含有Mg2+ | |
| B. | 滴入BaCl2溶液和稀硝酸,产生白色沉淀,则原溶液一定含有SO42- | |
| C. | 滴入稀硫酸产生无色无味使澄清石灰水浑浊的气体,则原溶液一定含有CO32- | |
| D. | 滴入KSCN溶液呈无色,再通入少量Cl2后呈红色,则原溶液一定含有Fe2+ |
分析 A.滴少量NaOH时生成白色沉淀可能为氢氧化镁、氢氧化铝等;
B.白色沉淀可能为AgCl或硫酸钡;
C.无色无味为二氧化碳;
D.滴入KSCN溶液呈无色,可知不含铁离子,再通入少量Cl2后呈红色,可知亚铁离子被氧化为铁离子.
解答 解:A.滴少量NaOH时生成白色沉淀可能为氢氧化镁、氢氧化铝等,则原溶液可能含有Mg2+,故A错误;
B.白色沉淀可能为AgCl,则原溶液可能含银离子或SO42-,但二者不能同时存在,故B错误;
C.无色气体可能为二氧化碳或二氧化硫,则溶液中可能含有CO32-或HCO3-,或二者都有,故C错误;
D.加入KSCN溶液无色,可知不含铁离子,再通入少量Cl2后呈红色,可知亚铁离子被氧化为铁离子,则该溶液中一定含有Fe2+,故D正确;
故选D.
点评 本题考查常见离子的检验,为高频考点,把握试剂、现象、结论为解答的关键,侧重分析与实验能力的考查,注意检验时排除干扰离子,题目难度不大.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | Ca(HCO3)2、Al(OH)3 | B. | Al(OH)3、NaHCO3 | C. | Na2SO3、Mg(OH)2 | D. | Na2CO3、CuSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图中新月形分子和环状分子“组合”在一起,铜离子起关键作用 | |
| B. | 利用此方式可以合成新分子,同时也可能创造一种全新“机械键” | |
| C. | 在创造新分子技术中,铜离子是唯一可以借助的金属离子 | |
| D. | 此技术可以“互锁”合成  分子,甚至成更复杂的分子 分子,甚至成更复杂的分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
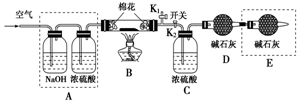 为探究所得的水合碱式碳酸镁[mMgCO3•nMg(OH)2•x
为探究所得的水合碱式碳酸镁[mMgCO3•nMg(OH)2•x查看答案和解析>>
科目:高中化学 来源: 题型:解答题
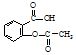 )具有解热镇痛作用(选填“解热镇痛”或“抗菌消炎”),必须密闭干燥存储以防止发生水解,在酸性条件下阿司匹林水解生成乙酸和
)具有解热镇痛作用(选填“解热镇痛”或“抗菌消炎”),必须密闭干燥存储以防止发生水解,在酸性条件下阿司匹林水解生成乙酸和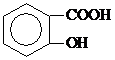 (写出结构简式).
(写出结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
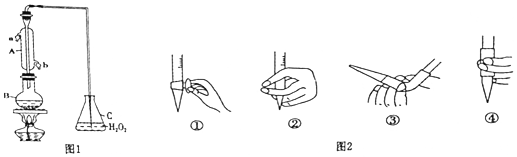
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (1)(2)(3)(5) | B. | (1)(3)(5) | C. | (2)(3)(6) | D. | (1)(3)(4)(5) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用小苏打治疗胃酸过多:HCO3-+H+═CO2↑+H2O | |
| B. | 纯碱溶液与石灰水反应:Ca2++CO32-=CaCO3↓ | |
| C. | 铜粉与硝酸银溶液反应:Ag++Cu═Ag+Cu2+ | |
| D. | 盐酸滴在石灰石上:CaCO3+2H+=Ca2++CO2↑+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com