
【题目】(1)甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源。在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为__。
(2)工业上一般可采用下列反应来合成甲醇:CO(g)+2H2(g)CH3OH(g),现实验室模拟该反应并进行分析,如图是该反应在不同温度下CO的转化率随时间变化的曲线。
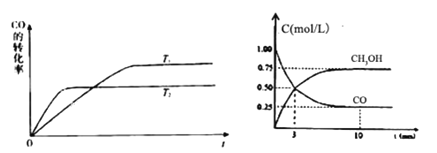
①该反应的焓变△H____0(填“>”“<”或“=”).
②T1和T2温度下的平衡常数大小关系是K1__K2(填“>”“<”或“=”)
③现进行如下实验,在体积为1L的密闭容器中,充入1molCO和3molH2,测得CO和CH3OH(g)的浓度随时间变化如图所示.从反应开始到平衡,CO的平均反应速率v(CO)=____,该反应的平衡常数为K=____。
【答案】CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l)ΔH=–725.76kJ·mol-1 < > 0.075mol/(Lmin) 4/3
【解析】
(1)在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ,则1mol甲醇(CH3OH)燃烧生成CO2和液态水时放热为:![]() ,则表示甲醇燃烧热的热化学方程式为:CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l)ΔH=–725.76kJ·mol-1。本小题答案为:CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l)ΔH=–725.76kJ·mol-1。
,则表示甲醇燃烧热的热化学方程式为:CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l)ΔH=–725.76kJ·mol-1。本小题答案为:CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l)ΔH=–725.76kJ·mol-1。
(2)①根据先拐先平数值大的原则,由第一个图可知,温度T1<T2,平衡时,温度越高CO的转化率越小,说明升高温度,平衡向逆反应方向移动,由于升高温度平衡向吸热反应方向移动,故该反应正反应为放热反应。本小题答案为:<。
②该反应正反应为放热反应,升高温度,平衡向逆反应移动,所以K1>K2。本小题答案为:>。
③由第二个图可知,10min达平衡时甲醇的浓度变化量为0.75mol/L,所以![]() ,由于速率之比等于化学计量数之比,所以
,由于速率之比等于化学计量数之比,所以![]() 。平衡时,c(CH3OH)为0.75mol/L,c(CO)的浓度为0.25mol/L,反应消耗一氧化碳浓度为0.75mol/L,则反应消耗氢气浓度为0.75mol/L×2=1.5mol/L,则达到平衡时氢气浓度为:c(H2)=3mol/L-1.5mol/L=1.5mol/L,所以该温度下该反应的平衡常数:
。平衡时,c(CH3OH)为0.75mol/L,c(CO)的浓度为0.25mol/L,反应消耗一氧化碳浓度为0.75mol/L,则反应消耗氢气浓度为0.75mol/L×2=1.5mol/L,则达到平衡时氢气浓度为:c(H2)=3mol/L-1.5mol/L=1.5mol/L,所以该温度下该反应的平衡常数:![]() 。本小题答案为:0.075mol/(Lmin) ;4/3。
。本小题答案为:0.075mol/(Lmin) ;4/3。


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
【题目】已知25 ℃时,Ka(HF)=6.0×10-4,Ksp(MgF2)=5.0×10-11。现向1 L 0.2 mol·L-1 HF溶液中加入 1 L 0.2 mol·L-1 MgCl2溶液。下列说法中正确的是( )
A. 25 ℃时,0.1 mol·L-1 HF溶液中pH=1
B. 0.2 mol·L-1 MgCl2溶液中离子浓度关系为2c(Mg2+)=c(Cl-)>c(H+)=c(OH-)
C. 2HF(aq)+Mg2+(aq)![]() MgF2(s)+2H+(aq),该反应的平衡常数K=1.2×107
MgF2(s)+2H+(aq),该反应的平衡常数K=1.2×107
D. 该反应体系中有MgF2沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:① A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平 ② 2CH3CHO+O2![]() 2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如图所示:
2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如图所示:
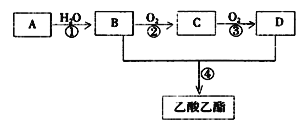
回答下列问题:
(1)B、D分子中的官能团名称分别是____、_____。
(2)写出下列反应的反应类型:①________,②__________,④_________。
(3)写出下列反应的化学方程式:
①__________;
②__________;
④__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的恒容密闭容器中,当下列哪些物理量不再发生变化时,表明下述反应:A(s) + 2B(g)![]() C(g) + D(g) 已达到平衡状态‘
C(g) + D(g) 已达到平衡状态‘
①混合气体的压强 ②混合气体的密度
③B的物质的量浓度 ④气体的总物质的量
⑤混合气体总质量
A. ②③⑤ B. ①②③ C. ②③④ D. ①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷、乙烯和苯都是重要的化工原料,请回答下列问题。
(1)甲烷的电子式为__________,写出在光照条件下,甲烷与氯气发生反应生成气态有机物的化学方程式:________。
(2)下列叙述不正确的是________
A. CH4与C4H10互为同系物 B. C5H12有3种同分异构体
C. 烷烃的卤代反应很难得到纯净物 D. 烷烃分子中,相邻的三个碳原子可能在同一条直线
(3) 下列物质不可能是乙烯加成产物的是(__________)
A. CH3CH3 B. CH3CHCl2 C. CH3CH2OH D. CH3CH2Br
(4)若将乙烯通入到紫色高锰酸钾溶液中,可以观察到__________,乙烯发生的反应类型为________。
(5) 苯的结构简式:________,它与液溴在催化剂作用下发生取代反应的化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近科学家获得了一种稳定性好、抗氧化能力强的活性化合物A;其结构如下:
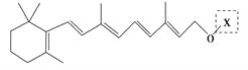
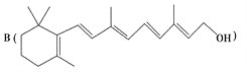
为了研究X的结构,将化合物A在一定条件下水解只得到B(结构如图所示)和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
请回答下列问题:
(1)化合物B能发生下列哪些类型的反应________。
A.取代反应 B.加成反应 C.缩聚反应 D.氧化反应
(2)写出化合物C所有可能的结构简式______________________________。
(3)C可通过下图所示途径合成,并制取冬青油和阿司匹林。
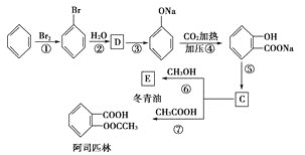
(ⅰ)写出有机物的结构简式:D:______________C______________ E _______________
(ⅱ)写出变化过程中①、⑥的化学方程式(注明反应条件)反应①_____________________;反应⑥_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“C1化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH、HCOOH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义。
(1)一定温度下,在两个容积均为2 L的密闭容器中,分别发生反应:
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。相关数据如下:
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。相关数据如下:
容器 | 甲 | 乙 |
反应物投入量 | 1molCO2(g)和 3molH2(g) | 1mol CH3OH (g)和 1molH2O(g) |
平衡时c(CH3OH) | c1 | c2 |
平衡时能量变化 | 放出29.4kJ | 吸收a kJ |
请回答:
①a=_______________;
②若甲中反应10 s时达到平衡,则用CO2来表示甲中反应从开始到平衡过程中的平均反应速率是___________。
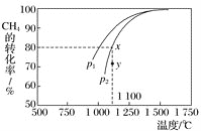
(2)甲烷的一个重要用途是制取H2,其原理为CO2(g)+CH4(g) ![]() 2CO(g)+2H2(g)。在密闭容器中通入等物质的量浓度的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图所示,则压强p1_____(填“大于”或“小于”)p2;压强为p2时,在y点:v(正)______(填“大于”“小于”或“等于”)v(逆)。
2CO(g)+2H2(g)。在密闭容器中通入等物质的量浓度的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图所示,则压强p1_____(填“大于”或“小于”)p2;压强为p2时,在y点:v(正)______(填“大于”“小于”或“等于”)v(逆)。
(3)一定条件下,治理汽车尾气的反应是2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g) ΔH<0。在恒温恒容的密闭容器中通入n(NO)∶n(CO)=2∶1的混合气体,发生上述反应。下列图像正确且能说明反应在进行到t1时刻一定达到平衡状态的是________(填字母)。
2CO2(g)+N2(g) ΔH<0。在恒温恒容的密闭容器中通入n(NO)∶n(CO)=2∶1的混合气体,发生上述反应。下列图像正确且能说明反应在进行到t1时刻一定达到平衡状态的是________(填字母)。
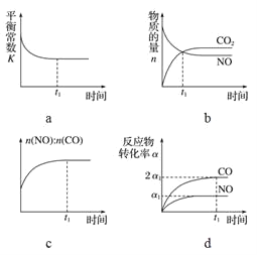
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质检验是化学研究常用的方法之一。下列有关溶液成分的检验,结论不正确的是
A.若滴加酚酞溶液,溶液变红,原溶液不一定是碱溶液
B.若先滴加足量新制氯水,再滴加少量KSCN溶液,溶液变为血红色,则原溶液一定含有Fe2+
C.若滴加Na2CO3溶液,产生白色沉淀,则原溶液可能含有Ca2+
D.若滴加稀盐酸,产生能使澄清石灰水变浑浊的气体,则原溶液中可能含CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼(Mo)是一种难熔稀有金属,我国的钼储量居世界第二,而云南钼的产量又居中国首位。钼及其合金在冶金、农业、电器、化工、环保等方面有着广泛的应用。
(1)Mo可被发烟硝酸氧化,产物MoOF4和MoO2F2物质的量比为1:1,完成下列方程式:_____Mo+_____HF+_____HNO3=_____MoO2F2+_____MoOF4+_____NO2↑+__________
(2)已知:
①2Mo(s)+3O2(g)=2MoO3(s)△H1
②MoS2(s)+2O2(g)═Mo(s)+2SO2(g)△H2
③2MoS2(s)+7O2(g)═2MoO3(s)+4SO2(g)△H3
则ΔH3=_____(用含ΔH1、ΔH2的代数式表示),在反应③中若有0.2molMoS2参加反应,则转移电子_________mol。
(3)密闭容器中用Na2CO3(s)作固硫剂,同时用一定量的氢气还原辉钼矿(MoS2)的原理为以下所示化学方程式MoS2(s)+4H2(g)+2Na2CO3(s)═Mo(s)+2CO(g)+4H2O(g)+2Na2S(s)△H
实验测得平衡时的有关变化曲线如图所示:

①由图可知,该反应的ΔH_____0(填“>”或“<”);P2_____0.1MPa(填“>”或“<”)。
②如果上述反应在体积不变的密闭容器中达到平衡,下列说法错误的是_____选填编号)
A.V正(H2)=V逆(H2O)
B.再加入MoS2,则H2转化率增大
C.容器内气体的密度不变时,一定达到平衡状态
D.容器内压强不变时,一定达到平衡状态
③由图可知M点时氢气的平衡转化率为_____(计算结果保留0.1%)。
④平衡常数可用平衡分压代替平衡浓度计算,气体分压=气体总压×物质的量分数。求图中M点的平衡常数Kp=_____(MPa)2。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com