
| A. | 正极,被还原 | B. | 正极,被氧化 | C. | 负极,被还原 | D. | 负极,被氧化 |
科目:高中化学 来源: 题型:填空题
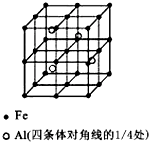 一种Al-Fe合金的立体晶胞结构如图,请据此回答下列问题:
一种Al-Fe合金的立体晶胞结构如图,请据此回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单离子半径:W<X<Z | |
| B. | W与X形成的化合物溶于水后溶液呈碱性 | |
| C. | 气态氢化物的热稳定性:W<Y | |
| D. | 最高价氧化物的水化物的酸性:Y>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势,如图所示:
反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势,如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学式 | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
| 颜色 | 白色 | 浅黄色 | 黄色 | 黑色 | 红色 |
| Ksp | 1.8×10-10 | 5.0×10-13 | 8.3×10-17 | 2.0×10-48 | 1.8×10-10 |
| A. | KBr | B. | KI | C. | K2S | D. | K2CrO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 图是甲烷燃料电池的结构示意图.甲烷在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为 CH4+2O2→CO2+2H2O.下列说法不正确的是( )
图是甲烷燃料电池的结构示意图.甲烷在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为 CH4+2O2→CO2+2H2O.下列说法不正确的是( )| A. | 左电极为电池的负极,a处通入的物质是甲烷 | |
| B. | 电池工作时外电路电子从负极流向正极,内电路电子从正极流向负极 | |
| C. | 负极反应式为:CH4+2H2O-8e-→CO2+8H+ | |
| D. | 正极反应式为:O2+4H++4e-→2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | A | B | C | D |
| 物质 | 加碘食盐 | 石英砂 | “84”消毒液 | 水玻璃 |
| 主要成分 | KIO3 | SiO2 | Ca(ClO)2 | NaSiO3 |
| 用途 | 预防碘缺乏病 | 作干燥剂 | 作消毒剂 | 木材防火剂 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
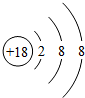 ,由2个原子组成的分子是HCl、由2原子组成具有10电子的阴离子OH-.
,由2个原子组成的分子是HCl、由2原子组成具有10电子的阴离子OH-.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com