
 甲醇(CH3OH)是一种优质燃料,
甲醇(CH3OH)是一种优质燃料,分析 (1)①根据n=$\frac{m}{M}$计算88gCO2和氢气化合生成甲醇和水放出的热量,结合热化学方程式书写方法标注物质聚集状态和反应焓变写出;
②反应热与化学计量数成正比,根据热化学方程式计算;
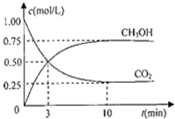
(2)在体积为l L的密闭容器中,充入l mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图2所示.二氧化碳是反应物随反应进行浓度减小,甲醇是生成物,随反应进行浓度增大;10nim内达到平衡,生成甲醇浓度为0.75mol/L,二氧化碳浓度变化了0.75mol/L;
①依据化学平衡三段式列式利用V=$\frac{△c}{△t}$计算;
②依据升温,增加浓度,加压,加催化剂等可以加快反应速率判断;
③可逆反应达到平衡状态时,正逆反应速率相等(同种物质)或正逆反应速率之比等于系数之比(不同物质),平衡时各种物质的物质的量、浓度等不再发生变化,由此衍生的一些物理量不变,以此分析解答.
解答 解:(1)①88gCO2的物质的量为n=$\frac{m}{M}$=$\frac{88g}{44g/mol}$=2mol,放出98kJ的热量,每1molCO2和足量氢气完全反应三可生成1mol气态甲醇(CH3OH)和1mol 水蒸汽并放出49kJ的热量,热化学方程式为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H=-49.0kJ/mol,
故答案为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H=-49.0kJ/mol;
②每1molCO2和足量氢气完全反应三可生成1mol气态甲醇(CH3OH)和1mol 水蒸汽并放出49kJ的热量,若生成3mol甲醇放出的热量为49kJ×3=147KJ,
故答案为:147KJ;
(2)在体积为l L的密闭容器中,充入l mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图2所示.二氧化碳是反应物随反应进行浓度减小,甲醇是生成物,随反应进行浓度增大;10nim内达到平衡,生成甲醇浓度为0.75mol/L,二氧化碳浓度变化了0.75mol/L;则①依据化学平衡列式计算为:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
起始量(mol/L) 1 3 0 0
变化量(mol/L) 0.75 2.25 0.75 0.75
平衡量(mol/L) 0.25 0.75 0.75 0.75
H2的平均反应速率v(H2)=$\frac{2.25mol/L}{10min}$=0.225mol•L-1•min-1 ;
故答案为:0.225mol•L-1•min-1 ;
②A.加入催化剂,v (CO2)增大,故A正确;
B.充入He(g),使体系压强增大,但反应物浓度不变,所以v (CO2)不变,故B错误;
C.将H2O(g)从体系中分离,则生成物浓度减小,则浓度减小,故C错误;
D.升高温度,v (CO2)增大,故D正确;
故选:AD;
③A.反应前后气体的体积不等,所以压强一直在变,则当压强不变时能说明达到平衡,故A正确;
B.反应前后质量不变,体积也不变,所以密度一直不变,则混合气体的密度不再变化不能说明达到平衡,故B错误;
C.CO2、H2和CH3OH的浓度不再变化,说明达到平衡,故C正确;
D.单位时间内消耗3molH2的同时生成1molCH3OH,都是指正反应方向,不能说明达到平衡,故D错误;
E.CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H=-49.0kJ/mol,CO2结构简式为O=C=O,1个分子有2个C=O键,当2个C=O键断裂的同时,必有3个H-H键断裂.与是否已达到平衡
无关,故E错误;
故选AC.
点评 本题考查了热化学方程式的书写原则,化学反应速率、平衡状态的判断以及化学平衡的计算的应用,图象分析是关键,综合性较大,难度中等.


科目:高中化学 来源: 题型:选择题
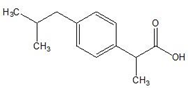 布洛芬缓释胶囊常用于缓解轻至中度疼痛如头痛、关节痛、偏头痛、牙痛、肌肉痛、神经痛、痛经.也用于普通感冒或流行性感冒引起的发热,布洛芬结构如图所示,下列关于布洛芬的说法正确的是( )
布洛芬缓释胶囊常用于缓解轻至中度疼痛如头痛、关节痛、偏头痛、牙痛、肌肉痛、神经痛、痛经.也用于普通感冒或流行性感冒引起的发热,布洛芬结构如图所示,下列关于布洛芬的说法正确的是( )| A. | 其分子式可以表示为C13H20O2 | |
| B. | 1mol该物质最多与4molH2加成 | |
| C. | 其核磁共振氢谱谱图有8个峰 | |
| D. | 该物质可发生氧化、还原、加成、消去、取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓盐酸与二氧化锰共热 | B. | 浓硫酸与铜共热 | ||
| C. | 过氧化钠与水反应 | D. | 石灰石与稀盐酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化氢的电子式为: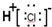 | |
| B. | 重氢负离子(${\;}_{1}^{2}$H-)的结构示意图为 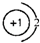 | |
| C. | 次氯酸的结构式为H-Cl-O | |
| D. | 氯化钠的分子式:NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器内气体的总质量不随时间而变化 | |
| B. | 单位时间内有nmolA2生成的同时就有nmolB2生成 | |
| C. | 2 v(A2)正=v(AB)逆 | |
| D. | A2、B2(g)、AB(g)的浓度之比为1:1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、K+、NO3-、Cl- | B. | K+、Na+、HS-、Cl- | ||
| C. | Na+、AlO2-、SO42-、NO3- | D. | Ba2+、Na+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{m}{A+16}$(A-n+8)mol | B. | $\frac{m}{A+16}$(A-n+10)mol | C. | (A-n+2)mol | D. | $\frac{m}{A}$(A-n+6)mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5 mol/(L•min) | B. | 1 mol/(L•min) | C. | 2 mol/(L•min) | D. | 3 mol/(L•min) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com