
”¾ĢāÄæ”æĘ½°åµēŹÓĻŌŹ¾ĘĮÉś²ś¹ż³ĢÖŠ²śÉś“óĮæµÄ·Ļ²£Į§(ŗ¬SiO2”¢Fe2O3”¢CeO2”¢FeOµČĪļÖŹ)”£Ä³Š”×éŅŌ“Ė·Ļ²£Į§ĪŖŌĮĻ£¬Éč¼ĘČēĻĀ¹¤ŅÕĮ÷³Ģ¶Ō׏Ō“½ųŠŠ»ŲŹÕ£¬µĆµ½Ce(OH)4”£

¼ŗÖŖ:CeO2²»ČÜÓŚĒæĖį»ņĒæ¼ī£»Ce3+Ņ×Ė®½ā£¬ĖįŠŌĢõ¼žĻĀ£¬Ce4+ÓŠĒæŃõ»ÆŠŌ”£
(1)·Ļ²£Į§ŌŚNaOHČÜŅŗ½žĻ“Ē°ĶłĶłŅŖ½ųŠŠµÄ²Ł×÷________£¬·“Ó¦¢ŁµÄĄė×Ó·½³ĢŹ½_______”£
(2)·“Ó¦¢ŚµÄĄė×Ó·½³ĢĪäŹĒ____________”£
(3)ĪŖĮĖµĆµ½½Ļ“æµÄCe3+ČÜŅŗ£¬·“Ó¦¢ŚÖ®Ē°ŅŖ½ųŠŠµÄ²Ł×÷ŹĒ______”£
(4)·“Ó¦¢ŪŠčŅŖ¼ÓČėµÄŹŌ¼ĮXæÉŅŌŹĒ_________”£
(5)ÓƵĪ¶Ø·Ø²ā¶ØÖʵƵÄCe(OH)4²śĘ·“æ¶Č”£
![]()
ÓĆFeSO4ČÜŅŗµĪ¶ØÓĆ_____×öÖøŹ¾¼Į£¬µĪ¶ØÖÕµćµÄĻÖĻó_______ČōĖłÓĆFeSO4ČÜŅŗŌŚæÕĘųÖŠĀ¶ÖĆŅ»¶ĪŹ±¼äŗóŌŁ½ų½ųŠŠµĪ¶Ø£¬Ōņ²āµĆøĆCe(OH)4²śĘ·µÄÖŹĮæ·ÖŹż____(Ģī”°Ę«“ó”±”¢”°Ę«Š””±»ņ”°ĪŽÓ°Ļģ”±)”£
”¾“š°ø”æ ·ŪĖé SiO2+2OH-=SiO32-+H2O 2CeO2+H2O2+6H+=2Ce3++O2”ü+4H2O Ļ“µÓ O2»ņĘäĖüŗĻĄķ“š°ø K3[Fe(CN)6] ×īŗóŅ»µĪČÜŅŗŹ±£¬Éś³ÉµĄ¶É«³Įµķ£¬ĒŅÕńµ“Ņ²²»ŌŁĻūŹ§ Ę«“ó
”¾½āĪö”æ·Ļ²£Į§·ŪÄ©(ŗ¬SiO2”¢Fe2O3”¢CeO2”¢FeOµČĪļÖŹ)¼ÓĒāŃõ»ÆÄĘČÜŅŗ£¬¶žŃõ»Æ¹čČÜÓŚĒāŃõ»ÆÄĘÉś³É¹čĖįÄĘ£¬Fe2O3”¢CeO2”¢FeO²»ČÜ£¬¹żĀĖ£¬µĆµ½ĀĖŅŗAµÄÖ÷ŅŖ³É·ÖĪŖ¹čĖįÄĘ£¬ĀĖŌüAµÄ³É·ÖŹĒFe2O3”¢CeO2”¢FeO£¬ĀĖŌüA(Fe2O3”¢CeO2”¢FeO)¼ÓĻ”ĮņĖįŗó¹żĀĖµĆĀĖŅŗBŹĒĮņĖįŃĒĢś”¢ĮņĖįĢśµÄ»ģŗĻČÜŅŗ£¬ĀĖŌüBµÄ³É·ÖŹĒCeO2£¬CeO2ÓėH2O2ŗĶĻ”H2SO4·“Ӧɜ³ÉCe3+ŗĶO2£¬·“Ó¦ĪŖ£ŗ2CeO2+H2O2+6H+=2Ce3++O2”ü+4H2O£»Ce3+¼Ó¼īÉś³ÉCe(OH)3Šü×ĒŅŗ£»Ce(OH)3Šü×ĒŅŗ±»Ńõ»ÆÉś³ÉCe(OH)4”£
(1)·Ļ²£Į§ŌŚNaOHČÜŅŗ½žĻ“Ē°ĶłĶłŅŖŠčŅŖ·ŪĖ飬æÉŅŌĢįøß½žČ”ĀŹŗĶ½žČ”ĖŁĀŹ£¬·“Ó¦¢ŁÖŠ¶žŃõ»Æ¹čČÜÓŚĒāŃõ»ÆÄĘÉś³É¹čĖįÄĘ£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖSiO2+2OH-=SiO32-+H2O£¬¹Ź“š°øĪŖ£ŗ·ŪĖ飻SiO2+2OH-=SiO32-+H2O£»
(2)·“Ó¦¢ŚĪŖCeO2ÓėH2O2ŗĶĻ”H2SO4·“Ӧɜ³ÉCe3+ŗĶO2£¬·“Ó¦ĪŖ£ŗ2CeO2+H2O2+6H+= 2Ce3++O2”ü+4H2O£»¹Ź“š°øĪŖ£ŗ2CeO2+H2O2+6H+=2Ce3++O2”ü+4H2O£»
(3)ĪŖĮĖµĆµ½½Ļ“æµÄCe3+ČÜŅŗ£¬·“Ó¦¢ŚÖ®Ē°ŠčŅŖĀĖŌüB½ųŠŠĻ“µÓ£¬¹Ź“š°øĪŖ£ŗĻ“µÓ£»
(4)øł¾ŻÉĻŹö·ÖĪö£¬·“Ó¦¢ŪÖŠCe(OH)3Šü×ĒŅŗ±»Ńõ»ÆÉś³ÉCe(OH)4£¬ŠčŅŖ¼ÓČėµÄŹŌ¼ĮXæÉŅŌŹĒO2£¬¹Ź“š°øĪŖ£ŗO2£»
(5) K3[Fe(CN)6]Äܹ»ÓėĮņĖįŃĒĢś·“Ӧɜ³ÉĢŲÕ÷µÄĄ¶É«³Įµķ£¬ÓĆFeSO4ČÜŅŗµĪ¶ØæÉŅŌÓĆK3[Fe(CN)6] ×öÖøŹ¾¼Į£¬µĪ¶ØÖÕµćµÄĻÖĻóĪŖ×īŗóŅ»µĪČÜŅŗŹ±£¬Éś³ÉµĄ¶É«³Įµķ£¬ĒŅÕńµ“Ņ²²»ŌŁĻūŹ§£»ĖłÓĆFeSO4ČÜŅŗŌŚæÕĘųÖŠĀ¶ÖĆŅ»¶ĪŹ±¼äŗóŌŁ½ųŠŠµĪ¶Ø£¬²æ·ÖŃĒĢśĄė×Ó±»Ńõ»ÆÉś³ÉĢśĄė×Ó£¬ŌņĮņĖįŃĒĢśÅØ¶Č½µµĶ£¬µ¼ÖĀĮņĖįŃĒĢśČÜŅŗĢå»żŌö“ó£¬ĖłŅŌ²āµĆøĆCe(OH)4²śĘ·µÄÖŹĮæ·ÖŹżĘ«“ó£»¹Ź“š°øĪŖ£ŗK3[Fe(CN)6]£»×īŗóŅ»µĪČÜŅŗŹ±£¬Éś³ÉµĄ¶É«³Įµķ£¬ĒŅÕńµ“Ņ²²»ŌŁĻūŹ§£»Ę«“ó”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĢ¼øśÅØĮņĖį¹²ČČ²śÉśµÄĘųĢåXŗĶĶøśÅØĻõĖį·“Ó¦²śÉśµÄĘųĢåYĶ¬Ź±ĶØČėŹ¢ÓŠ×ćĮæĀČ»Æ±µČÜŅŗµÄĻ“ĘųĘæÖŠ£ØČēĶ¼×°ÖĆ£©£¬ĻĀĮŠĖµ·ØŹĒÕżČ·µÄŹĒ

A. Ļ“ĘųĘæÖŠ²śÉśµÄ³ĮµķŹĒĢ¼Ėį±µ
B. “ÓZµ¼¹Ü³öĄ“µÄĘųĢåÖŠĪŽ¶žŃõ»ÆĢ¼
C. Ļ“ĘųĘæÖŠ²śÉśµÄ³ĮµķŹĒĢ¼Ėį±µŗĶĮņĖį±µµÄ»ģŗĻĪļ
D. Zµ¼¹ÜæŚÓŠŗģ×ŲÉ«ĘųĢå³öĻÖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŗĻ³ÉŠĀŠĶøß·Ö×ÓMµÄĀ·ĻßČēĶ¼£ŗ 
ĪŖĮĖ²ā¶ØÉĻŹö×Ŗ»ÆĮ÷³ĢÖŠÓŠ»śĪļHµÄ½į¹¹£¬×öČēĻĀŹµŃé£ŗ
¢Ł½«2.3gÓŠ»śĪļHĶźČ«Č¼ÉÕ£¬Éś³É0.1molCO2ŗĶ2.7gĖ®
¢ŚHµÄÖŹĘ×Ķ¼ŗĶŗĖ“Ź²ÕńĒāĘ×Ķ¼·Ö±šĪŖĶ¼1ŗĶĶ¼2£ŗ 
ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ÓŠ»śĪļHÖŠ¹ŁÄÜĶŵÄĆū³Ę £®
£Ø2£©AµÄ·Ö×ÓŹ½ŹĒC7H8 £¬ ·“Ó¦¢ŁµÄ»Æѧ·½³ĢŹ½£ŗ £®
£Ø3£©EµÄ·Ö×ÓŹ½ŹĒC6H10O2 £¬ EµÄ½į¹¹¼ņŹ½ĪŖ £®
£Ø4£©ŹŌ¼ĮbŹĒ £¬ ·“Ó¦¢ÜµÄ·“Ó¦ĄąŠĶŹĒ £®
£Ø5£©·“Ó¦¢ŽµÄ»Æѧ·½³ĢŹ½£ŗ £®
£Ø6£©ŅŃÖŖ£ŗ ŅŌHĪŖĘšŹ¼ŌĮĻ£¬Ń”ÓƱŲŅŖµÄĪŽ»śŹŌ¼ĮŗĻ³ÉE£¬Š“³öŗĻ³ÉĀ·ĻߣØÓĆ½į¹¹¼ņŹ½±ķŹ¾ÓŠ»śĪļ£¬ÓĆ¼żĶ·±ķŹ¾×Ŗ»Æ¹ŲĻµ£¬¼żĶ·ÉĻ×¢Ć÷ŹŌ¼ĮŗĶ·“Ó¦Ģõ¼ž£© £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻÖÓŠČż×é»ģŗĻĪļ£ŗ¢ŁCCl4 ŗĶĖ® ¢Ś45%µÄ¾Ę¾«Ė®ČÜŅŗ ¢ŪµāĖ®£¬Óū·ÖĄėø÷×é»ģŗĻĪļ£¬²ÉÓƵÄÖ÷ŅŖ·½·ØŅĄ“ĪŹĒ£Ø £©
A.Čܽā”¢¹żĀĖ ”¢½į¾§B.·ÖŅŗ”¢ÕōĮó”¢ŻĶČ”
C.ŻĶČ””¢·ÖŅŗ”¢ÕōĮóD.ÕōĮ󔢷ÖŅŗ”¢ŻĶČ”
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹ®¾Å“ó±ØøęÖø³ö£¬”°½ØÉčÉśĢ¬ĪÄĆ÷ŹĒÖŠ»ŖĆń×åĖ®Šų·¢Õ¹µÄĒ§Äź“ó¼Ę”±”£æŲÖĘŗĶÖĪĄķNOx”¢SO2”¢CO2ŹĒ½ā¾ö¹ā»ÆѧŃĢĖć”¢¼õÉŁĖįÓźŗĶĪĀŹŅŠ§Ó¦µÄÓŠŠ§Ķ¾¾¶£¬¶Ō¹¹½ØÉśĢ¬ĪÄĆ÷ӊ׿«ĪŖÖŲŅŖµÄŅāŅ唣»Ų“šĻĀĮŠĪŹĢā:
(1)ĄūÓĆSCRŗĶNSR¼¼ŹõæÉÓŠŠ§½µµĶ²ńÓĶ·¢¶Æ»śŌŚæÕĘų¹żĮæĢõ¼žĻĀµÄNOxÅÅ·Å”£
¢ŁSCR(Ń”Ōń“߻ƻ¹ŌNOx)¹¤×÷ŌĄķ:
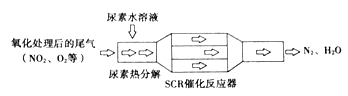
ÄņĖŲĖ®ČÜŅŗČČ·Ö½āĪŖNH3ŗĶCO2µÄ»Æѧ·½³ĢŹ½ĪŖ________,SCR“߻Ʒ“Ó¦Ę÷ÖŠNH3»¹ŌNO2µÄ»Æѧ·½³ĢŹ½ĪŖ__________”£
¢ŚNSR(NOx“¢“ę»¹Ō)¹¤×÷ŌĄķ:
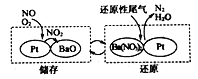
ŌŚ“¢“ę¹ż³ĢÖŠ,NO·¢ÉśµÄ×Ü»Æѧ·“Ó¦·½³ĢŹ½ĪŖ__________
(2)Ė«¼ī·Ø³żČ„SO2µÄ¹¤×÷ŌĄķ:NaOHČÜŅŗ![]() Na2SO3ČÜŅŗ
Na2SO3ČÜŅŗ
¹ż³Ģ¢ŁµÄĄė×Ó·½³ĢŹ½ĪŖ_____;CaOŌŚĖ®ÖŠ“ęŌŚČēĻĀ×Ŗ»Æ:CaO(s)+H2O(1)=Ca(OH)2(s)![]() Ca2+(aq)+2OH-(aq),“ÓĘ½ŗāŅĘ¶ÆµÄ½Ē¶Č£¬¼ņŹö¹ż³Ģ¢ŚNaOHŌŁÉśµÄŌĄķ____________.
Ca2+(aq)+2OH-(aq),“ÓĘ½ŗāŅĘ¶ÆµÄ½Ē¶Č£¬¼ņŹö¹ż³Ģ¢ŚNaOHŌŁÉśµÄŌĄķ____________.
(3)ČĖ¹¤¹āŗĻ×÷ÓĆ¼¼Źõ»ŲŹÕĄūÓƶžŃõ»ÆĢ¼µÄ¹¤×÷ŌĄķ:
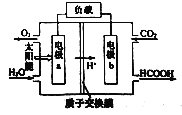
a¼«ĪŖ_______¼«,b¼«µÄµē¼«·“Ó¦Ź½ĪŖ______________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ3.6 gĢ¼ŌŚ6.4 gŃõĘųÖŠČ¼ÉÕ£¬ÖĮ·“Ó¦Īļŗľ”£¬²āµĆ·Å³öČČĮæa kJ”£ÓÖÖŖ12.0 gĢ¼ĶźČ«Č¼ÉÕ£¬·Å³öČČĮæĪŖ b kJ”£ŌņČČ»Æѧ·½³ĢŹ½C(s)£«![]() O2(g)===CO(g)””¦¤H£½Q ÖŠQµČÓŚ(”””” )
O2(g)===CO(g)””¦¤H£½Q ÖŠQµČÓŚ(”””” )
A. £(a£b) kJ”¤mol£1 B. £(a£«b) kJ”¤mol£1
C. £(5a£0.5b) kJ”¤mol£1 D. £(10a£b) kJ”¤mol£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠ¹ŲČēĶ¼ĖłŹ¾Ōµē³ŲµÄŠšŹö,ÕżČ·µÄŹĒ(ŃĪĒÅ֊װӊŗ¬Ēķ½ŗµÄKCl±„ŗĶČÜŅŗ)(””””)
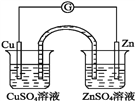
A. ĶʬÉĻ·¢ÉśŃõ»Æ·“Ó¦ B. Č”³öŃĪĒÅŗó,µēĮ÷¼ĘŅĄČ»·¢ÉśĘ«×Ŗ
C. ·“Ó¦ÖŠ,ŃĪĒÅÖŠµÄK+»įŅĘĻņCuSO4ČÜŅŗ D. ·“Ó¦Ē°ŗóĶʬ֏Įæ²»øıä
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚÉś²śŗĶÉś»īÖŠÓ¦ÓƵĻÆѧÖŖŹ¶ÕżČ·µÄŹĒ
A. ²£Į§”¢Ė®Äą”¢Ė®¾§ĻīĮ“¶¼ŹĒ¹čĖįŃĪÖĘĘ·
B. ¾§Ģå¹čŹĒŌŚĶ؊Ź¤³ĢÖŠÖĘ×÷¹āµ¼ĻĖĪ¬µÄÖ÷ŅŖŌĮĻ
C. Ģ¼ĖįÄĘŌŚŅ½ĮĘÉĻŹĒÖĪĮĘĪøĖį¹ż¶ąµÄŅ»ÖÖŅ©¼Į
D. ·¢½Ķ·ŪÖŠÖ÷ŅŖŗ¬ÓŠĢ¼ĖįĒāÄĘ£¬ÄÜŹ¹±ŗÖĘ³öµÄøāµćŹčĖɶąæ×
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚÓŠ»ś»Æѧ֊£¬Ķ¬·ÖŅģ¹¹ŹĒĘÕ±é“ęŌŚĻÖĻó£®·Ö×ÓŹ½ĪŖC4H9BrµÄÓŠ»śĪļ¹²ÓŠÖÖ£®ĘäÖŠ£¬Ņ»ÖÖÓŠ»śĪļĶعżĻūČ„·“Ó¦æÉ×Ŗ±äĪŖ2©¶”Ļ©£¬ĒėŠ“³öøĆĻūČ„·“Ó¦µÄ»Æѧ·½³ĢŹ½ £¬ ĮķŅ»ÖÖÓŠ»śĪļµÄŗĖ“Ź²ÕńĒāĘ×Ķ¼£Ø1HŗĖ“Ź²ÕńĘ×Ķ¼£©ÖŠĻŌŹ¾Ņ»øö·å£¬ĒėŠ“³öøĆÓŠ»śĪļµÄ½į¹¹¼ņŹ½ £®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com