
 2C(g)ŌŚ¶ØČŻĆܱÕČŻĘ÷ÖŠ“ļµ½Ę½ŗāµÄ±źÖ¾µÄŹĒ£ŗ¢ŁCµÄÉś³ÉĖŁĀŹÓėCµÄ·Ö½āĖŁĀŹĻąµČ£»¢Śµ„Ī»Ź±¼äÄŚamol AÉś³É£¬Ķ¬Ź±Éś³É3amolB£»¢ŪA”¢B”¢CµÄÅØ¶Č²»ŌŁ±ä»Æ£»¢Ü»ģŗĻĘųĢåµÄ×ÜŃ¹Ēæ²»ŌŁ±ä»Æ£»¢Ż»ģŗĻĘųĢåµÄĘ½¾łÄ¦¶ūÖŹĮæ²»ŌŁ±ä»Æ£»¢ŽÓĆA”¢B”¢CµÄĪļÖŹµÄĮæÅØ¶Č±ä»Æ±ķŹ¾µÄ·“Ó¦ĖŁĀŹÖ®±ČĪŖ1:3:2£»¢ßA”¢B”¢CµÄ·Ö×ÓŹżÄæ±ČĪŖ1:3:2£»¢ą»ģŗĻĘųĢåµÄĆÜ¶Č²»ŌŁ±ä»Æ
2C(g)ŌŚ¶ØČŻĆܱÕČŻĘ÷ÖŠ“ļµ½Ę½ŗāµÄ±źÖ¾µÄŹĒ£ŗ¢ŁCµÄÉś³ÉĖŁĀŹÓėCµÄ·Ö½āĖŁĀŹĻąµČ£»¢Śµ„Ī»Ź±¼äÄŚamol AÉś³É£¬Ķ¬Ź±Éś³É3amolB£»¢ŪA”¢B”¢CµÄÅØ¶Č²»ŌŁ±ä»Æ£»¢Ü»ģŗĻĘųĢåµÄ×ÜŃ¹Ēæ²»ŌŁ±ä»Æ£»¢Ż»ģŗĻĘųĢåµÄĘ½¾łÄ¦¶ūÖŹĮæ²»ŌŁ±ä»Æ£»¢ŽÓĆA”¢B”¢CµÄĪļÖŹµÄĮæÅØ¶Č±ä»Æ±ķŹ¾µÄ·“Ó¦ĖŁĀŹÖ®±ČĪŖ1:3:2£»¢ßA”¢B”¢CµÄ·Ö×ÓŹżÄæ±ČĪŖ1:3:2£»¢ą»ģŗĻĘųĢåµÄĆÜ¶Č²»ŌŁ±ä»Æ

 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 Z(g)£¬¾60 s“ļµ½Ę½ŗā£¬Éś³É0.3 mol Z£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ( )
Z(g)£¬¾60 s“ļµ½Ę½ŗā£¬Éś³É0.3 mol Z£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ( )| A£®ČōÉżøßĪĀ¶Č£¬XµÄĢå»ż·ÖŹżŌö“ó£¬ŌņÕż·“Ó¦ĪŖĪüČČ·“ |
| B£®½«ČŻĘ÷Ģå»ż±äĪŖ20 L£¬ZµÄĘ½ŗāÅØ¶Č±äĪŖŌĄ“µÄ1/2 |
| C£®ČōŌö“óŃ¹Ē棬ŌņĪļÖŹYµÄ×Ŗ»ÆĀŹ¼õŠ” |
| D£®ŅŌXÅØ¶Č±ä»Æ±ķŹ¾µÄ·“Ó¦ĖŁĀŹĪŖ0.001 mol/(L”¤s) |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
 xC(g)£¬2minŹ±·“Ó¦“ļµ½Ę½ŗāדĢ¬(ĪĀ¶Č²»±ä)£¬Ź£ÓąĮĖO£®8 mol B£¬²¢²āµĆCµÄÅضČĪŖO£®4 mol£ÆL£¬ĒėĢīŠ“ĻĀĮŠæÕ°×£ŗ
xC(g)£¬2minŹ±·“Ó¦“ļµ½Ę½ŗāדĢ¬(ĪĀ¶Č²»±ä)£¬Ź£ÓąĮĖO£®8 mol B£¬²¢²āµĆCµÄÅضČĪŖO£®4 mol£ÆL£¬ĒėĢīŠ“ĻĀĮŠæÕ°×£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
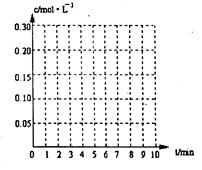
| | A | B | C | D |
| SO3 | 1mol | 3mol | 3mol | 0mol |
| SO2 | 2mol | 1.5mol | 0mol | 6mol |
| O2 | 2mol | 1mol | 0mol | 5mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
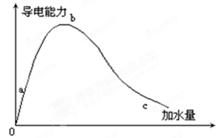
 Br2(g)+H2(g)£¬ŌŚĖÄÖÖ²»Ķ¬µÄĢõ¼žĻĀ½ųŠŠ£¬Br2”¢H2ĘšŹ¼µÄÅضČĪŖ0£¬·“Ó¦ĪļHBrµÄÅØ¶Č£Ømol/L£©Ėę·“Ó¦Ź±¼ä£Ømin£©µÄ±ä»ÆĒéæöČēĻĀ±ķ£ŗ
Br2(g)+H2(g)£¬ŌŚĖÄÖÖ²»Ķ¬µÄĢõ¼žĻĀ½ųŠŠ£¬Br2”¢H2ĘšŹ¼µÄÅضČĪŖ0£¬·“Ó¦ĪļHBrµÄÅØ¶Č£Ømol/L£©Ėę·“Ó¦Ź±¼ä£Ømin£©µÄ±ä»ÆĒéæöČēĻĀ±ķ£ŗ| ŹµŃéŠņŗÅ | ŹµŃéĪĀ¶Č | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800”ę | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800”ę | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800”ę | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820”ę | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
 Br2(g)+H2(g)Õż·“Ó¦ĪŖ·ÅČČ·“Ó¦
Br2(g)+H2(g)Õż·“Ó¦ĪŖ·ÅČČ·“Ó¦²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®¢Ł¢Ū | B£®¢Ł¢Ü | C£®¢Ś¢Ū | D£®¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
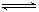 CO2(g)£«H2(g) ¦¤H <0,200”ꏱ£¬øĆ·“Ó¦µÄĘ½ŗā³£ŹżĪŖ1/2.25,øĆĪĀ¶ČĻĀ£¬½«Ņ»¶ØĮæµÄCOŗĶH2Ķ¶Čėij10LĆܱÕČŻĘ÷£¬5minŹ±“ļĘ½ŗā£¬ø÷ĪļÖŹÅضČ(mol?L”Ŗ1)±ä»ÆČēĻĀ£ŗ
CO2(g)£«H2(g) ¦¤H <0,200”ꏱ£¬øĆ·“Ó¦µÄĘ½ŗā³£ŹżĪŖ1/2.25,øĆĪĀ¶ČĻĀ£¬½«Ņ»¶ØĮæµÄCOŗĶH2Ķ¶Čėij10LĆܱÕČŻĘ÷£¬5minŹ±“ļĘ½ŗā£¬ø÷ĪļÖŹÅضČ(mol?L”Ŗ1)±ä»ÆČēĻĀ£ŗ| | 0min | 5min | 10min |
| CO | 0.01 | | 0.0056 |
| H2O | 0.01 | | 0.0156 |
| CO2 | 0 | | 0.0044 |
| H2 | 0 | | 0.0044 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®·²ŹĒģŹ±äŠ”ÓŚĮćµÄ·“Ó¦¶¼ÄÜ×Ō·¢½ųŠŠ |
| B£®·²ŹĒģŲ±äŠ”ÓŚĮćµÄ»Æѧ·“Ó¦¶¼ÄÜ×Ō·¢½ųŠŠ |
| C£®·²ŹĒģŹ±äŠ”ÓŚĮć£¬ģŲ±ä“óÓŚĮćµÄ»Æѧ±ä»Æ¶¼ÄÜ×Ō·¢½ųŠŠ |
| D£®CaCO3ŌŚøßĪĀĻĀµÄ·Ö½ā·“Ó¦²»ŹōÓŚ×Ō·¢¹ż³Ģ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com