
【题目】A、B、C、D四种元素,它们原子的核电荷数均小于18,且依次增大,A原子核内仅有一个质子;B原子的电子总数与D原子的最外层电子数相等;A原子与B原子最外层电子数之和与C原子的最外层电子数相等;D原子有两个电子层,最外层龟子数是次外层电子数的3倍。
(1)试推断它们各是什么元素? 按要求写出合适的化学用语:A的元素符号:______,C单质的电子式:_________________,用电子式表示D的简单氢化物的形成过程________。
(2)甲、乙、丙、丁是由以上四种元素中的几种组成的10 电子微粒;
①甲为分子,且为天然气的主要成分,则甲的化学式为______
②乙为气体,且遇到无色酚酞溶液变成红色,则乙的电子式为_______
③丙为阳离子,丁为阴离子,且丙和丁在加热条件下生成的两种物质也是10电子微粒,请写出该反应的离子方程式_______________。
【答案】H ![]()
![]() CH4
CH4 ![]() NH4++OH-
NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
【解析】
A的原子核中只有一个质子,则A的原子序数为1,A为H元素。D原子有两个电子层,最外层电子数是次外层电子数的3倍,分别是K层和L层,K层填满容纳2个电子,L层的电子数为K层的3倍,L层中的电子数为6;可知D元素为O元素。B的电子总数等于D的最外层电子数,B的电子总数为6,电子数等于原子序数,则B为6号元素,是C元素,B、C、D元素原子序数增大,B为C元素,D为O元素,则C为N元素。
(1) A的原子核中只有一个质子,则A的原子序数为1,A为H元素,A的元素符合为H。C为N元素,其单质为N2。N最外层只有5个电子,需要形成3对共用电子对,才能达到8电子稳定结构,因此N和N之间有3对共用电子对,则其电子式为![]() 。D为O元素,其简单氢化物为H2O,H2O为共价化合物,2个H原子和1个O原子,通过共用电子对生成水,用电子式表示为
。D为O元素,其简单氢化物为H2O,H2O为共价化合物,2个H原子和1个O原子,通过共用电子对生成水,用电子式表示为![]() ;
;
(2)H与C、N、O三种元素形成10电子的物质包括CH4、NH3、H2O、NH4+、H3O+、OH-等。
①甲为天然气的主要成分,天然气的主要成分为CH4,为10电子的分子,甲的分子式为CH4;
②乙遇无色的酚酞变红色,说明其溶液呈现碱性,高中阶段的唯一的碱性气体为NH3,N最外为5个电子,达到稳定结构需要形成3对共用电子对,恰好与3个氢原子形成3对共用电子对,其电子式为![]() ;
;
③阴阳离子反应而且产物均为10电子的物质,它们的反应为NH4+和OH-的反应。答案为NH4++OH-![]() NH3↑+H2O。
NH3↑+H2O。


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】已知: ①1mol晶体硅中含有2molSi-Si键。②Si(s)+O2(g)=SiO2(s)ΔH,其反应过程与能量变化如图所示。
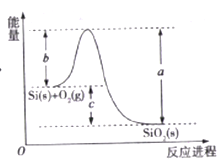
③
化学键 | Si-O | O=O | Si-Si |
断开1mol共价键所需能量/KJ | 460 | 500 | 176 |
下列说法正确的是
A. 晶体硅光伏发电是将化学能转化为电能的
B. 二氧化硅稳定性小于硅的稳定性
C. ΔH=-988 kJ/mol
D. ΔH=a-c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关生活中常见的物质,说法正确的是( )
A. 苯分子中的化学键是单双键交替结构 B. 聚乙烯能和溴水发生加成反应
C. 所有的糖类都能水解 D. 75%的酒精可以用于医疗杀菌消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的ΔH表示生成1 mol产物的数据)。
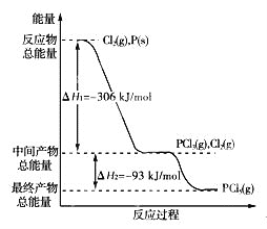
根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式是________________________________________;
(2)PCl5分解成PCl3和Cl2的热化学方程式是_________________________。
(3)P和Cl2分两步反应生成1 mol PCl5的反应热ΔH3= ___________,P和Cl2一步反应生成1 mol PCl5的ΔH4 ____________ΔH3(填“大于”、“小于”或“等于”);
(4)PCl5与足量水充分反应,最终生成两种酸,其化学方程式是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 盐酸与
盐酸与![]() 溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。
溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。

回答下列问题:
(1)从实验装置上看,图中尚缺少一种玻璃仪器,这种玻璃仪器的名称是____________________。能否改用铜丝_______(填“能、否”),原因是____________________________
(2)大烧杯上如不盖硬纸板,测得的中和热数值会__________(填“偏大”“偏小”或“无影响”)。
(3)实验中改用![]() 盐酸跟
盐酸跟![]() 溶液进行反应,与上述实验相比,所放出的热量__________(填“偏大”“相等”或“偏小”),所求中和热__________(填“相等”或“不相等”)。
溶液进行反应,与上述实验相比,所放出的热量__________(填“偏大”“相等”或“偏小”),所求中和热__________(填“相等”或“不相等”)。
(4)用相同浓度和体积的氨水代替![]() 溶液进行上述实验,测得的中和热数值会__________(填“偏大”“偏小”或“无影响”)。
溶液进行上述实验,测得的中和热数值会__________(填“偏大”“偏小”或“无影响”)。
(5)取![]() 溶液和
溶液和![]() 硫酸溶液进行实验,实验数据如下表。
硫酸溶液进行实验,实验数据如下表。
温度 实验次数 | 起始温度 | 终止温度
| 温度差平均值
| ||
|
| 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | _________________ |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
则中和热![]() __________(取小数点后一位。)(本题中
__________(取小数点后一位。)(本题中![]() 溶液和硫酸溶液的密度均取
溶液和硫酸溶液的密度均取![]() ,中和后生成溶液的比热容取
,中和后生成溶液的比热容取![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】茅台酒中存在少量具有凤梨香味的物质X,其结构如图所示。下列说法正确的是

A. X难溶于乙醇
B. 酒中的少量丁酸能抑制X的水解
C. 分子式为C4H8O2且官能团与X相同的物质有5种
D. X完全燃烧后生成CO2和H2O的物质的量比为1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 澄清石灰水与过量的小苏打溶液反应:Ca2++OH-+HCO3-===CaCO3↓+H2O
B. 酸性高锰酸钾溶液与稀草酸反应:5C2O42-+2MnO4-+16H+===2Mn2++10CO2+8H2O
C. AgCl的悬浊液中滴加Na2S溶液:2AgCl+S2-===Ag2S+2Cl-
D. NH4HCO3溶液加入过量NaOH溶液加热:NH4++OH-===NH3H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com